同周期的X、Y、Z三种元素,已知其高价氧化物对应的水化物的酸性强弱顺序是:
HXO4>H2YO4>H3ZO4,则下列各判断中正确的是 ( )
| A.原子半径:X>Y>Z | B.单质的非金属性:X>Y>Z |
| C.气态氢化物稳定性:X<Y<Z | D.原子序数:X>Y>Z |
在一定温度下,向a L密闭容器中加入1mol X气体和2mol Y气体,发生如下反应:X(g)+2Y(g)  2Z(g),此反应达到平衡的标志是
2Z(g),此反应达到平衡的标志是
| A.容器内气体密度不随时间变化 |
| B.v (X): v (Y)= l:2 |
| C.容器内X、Y、Z的浓度不随时间变化 |
| D.单位时间消耗0.1 molX同时生成0.2molZ |
一定条件下,反应4NH3(g)+5O2(g)  4NO(g)+6H2O(g)在5 L密闭容器中进行,10s后H2O的物质的量增加了0.60 mol,则10s内反应的平均速率
4NO(g)+6H2O(g)在5 L密闭容器中进行,10s后H2O的物质的量增加了0.60 mol,则10s内反应的平均速率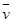 (X)可表示为 ()
(X)可表示为 ()
A.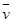 (NH3)=0.008 mol/(L·s) (NH3)=0.008 mol/(L·s) |
B.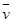 (NO)=0.04 mol/(L·s) (NO)=0.04 mol/(L·s) |
C.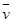 (O2)=0.006 mol/(L·s) (O2)=0.006 mol/(L·s) |
D.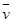 (H2O)=0.06 mol/(L.min) (H2O)=0.06 mol/(L.min) |
海水中含有的氯化镁是镁的重要来源之一。从海水中制取镁有多种生产方法,可按如下步骤进行:①把贝壳制成石灰乳②在引入的海水中加石灰乳,沉降、过滤、洗涤沉淀物③将沉淀物与盐酸反应,结晶、过滤、干燥产物④将得到的产物熔融后电解
关于从海水中提取镁的下列说法不正确的是( )
| A.此法的优点之一是原料来源丰富 |
| B.进行①②③步骤的目的是从海水中提取氯化镁 |
| C.第④步电解制镁是由于镁是很活泼的金属 |
| D.以上制取镁的过程中涉及的反应有分解反应、化合反应和置换反应 |
把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池。对该电池的描述合理的是()
①溶液中硫酸的物质的量浓度保持不变
②Cu极上有气泡产生,发生还原反应
③Cu为负极,Zn为正极
④原电池在工作时电子由负极通过溶液流向正极
⑤该装置将化学能转变为电能
| A.②⑤ | B.③⑤ | C.①② | D.④⑤ |