能用离子方程式H++OH-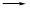 H2O表示的反应是
H2O表示的反应是
| A.稀醋酸和稀氨水反应 | B.稀硫酸和烧碱溶液反应 |
| C.稀盐酸和氢氧化铜反应 | D.稀硫酸和氢氧化钡溶液反应 |
为提纯下列物质(括号内物质为杂质),所选用的试剂和分离方法都正确的是
| 物质 |
除杂试剂 |
分离方法 |
|
| A |
Cu(Fe) |
稀硫酸 |
过滤 |
| B |
Cl2(HCl) |
NaOH溶液 |
洗气 |
| C |
I2(CCl4) |
—— |
过滤 |
| D |
Br2(H2O) |
酒精 |
萃取 |
下列反应中氯元素全部被还原的是
| A.NH3·H2O +HCl = NH4Cl+ H2O |
| B.Cl2+H2O = HCl+HClO |
| C.Cl2+2KI = 2KCl+I2 |
D.MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑ MnCl2+2H2O+Cl2↑ |
下列几种物质的保存方法中,不妥的是
| A.漂白粉可以在敞口容器中长期存放 |
| B.氯水保存在棕色瓶里并放在冷暗处 |
| C.液氯保存在绿色的干燥钢瓶中 |
| D.溴水盛放在有玻璃塞的细口瓶中 |
下列各种描述中,正确的是
| A.氯水具有杀菌消毒作用,其中起作用的物质是氯气 |
| B.加碘食盐中所加的“碘”一般是碘化钾 |
| C.区别氯化铁溶液和氢氧化铁胶体可以用丁达尔效应 |
| D.用干燥的有色布条可以检验氯化氢气体中是否混有氯气 |
下列物质中,所含分子的物质的量最多的是
| A.0.05 mol CCl4 |
| B.4℃ [ ρ(H2O)=1g·mL-1 ] 时,3.6 mL H2O |
| C.6.02×1022个HCl分子 |
| D.标准状况下,58.5 g的NaCl晶体 |