某课外兴趣小组对H2O2的分解速率做了如下实验探究。下表是该小组研究影响过氧化氢分解速率的因素时采集的一组数据:用10 mL H2O2制取150 mL O2所需的时间(秒)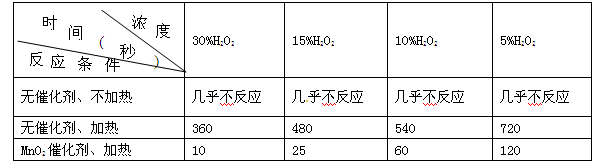
(1)该研究小组在设计方案时,考虑了浓度、____________、____________等因素对过氧化氢分解速率的影响;
(2)若已知1 克液态过氧化氢分解成氧气和液态水时,可放出2.89 kJ能量,写出该反应的热化学方程式:____________________;
(3)产生的O2充入某密闭容器,发生4NH3(g)+5O2(g) 4NO(g)+6H2O(g),不同情况测得反应速率,其中反应速率最快的是_________
4NO(g)+6H2O(g),不同情况测得反应速率,其中反应速率最快的是_________
| A.υ(NH3)="0.4" mol / (L·s) |
| B.υ(O2)="0.5" mol / (L·s) |
| C.υ(NO)="0.6" mol / (L·s) |
| D.υ(H2O)="1" mol / (L·min) |
水溶液中存在多种平衡,请根据所学化学知识回答下列问题:
(1)在浓度均为0.1mol/L①CH3COONH4②NH4HSO4③NH3.H2O ④(NH4)2SO4溶液中,NH4+浓度由大到小的顺序为(填序号)
(2)浓度均为0.1 mol·L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号) 。
(3)恒温下,向pH=6的蒸馏水中加入2.3g金属钠,充分反应后,再加蒸馏水稀释到1L,所得溶液的pH=。
铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得.
①铝土矿的主要成分是Al2O3和SiO2等.从铝土矿中提炼Al2O3的流程如图1所示: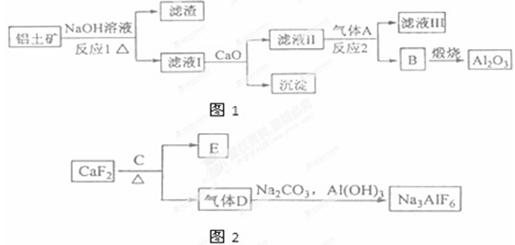
②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如图2所示:
回答下列问题:
(1)写出反应1的化学方程式_____________、__________;
(2)滤液Ⅰ中加入 生成的沉淀是_______,若通入的气体A少量则反应2的离子方程式为_____________。
生成的沉淀是_______,若通入的气体A少量则反应2的离子方程式为_____________。
(3)E常用作制作豆腐的添加剂,化合物C是____,写出由D制备冰晶石的化学方程式______________;
(1)在反应2KMnO4+16HBr===5Br2+2MnBr2+2KBr+8H2O中,还原剂是________。
(2)已知BrFx与H2O按物质的量之比3∶5反应的产物是HF、HBrO3、Br2、O2,该反应中的氧化剂是________,还原剂是________,BrFx中的x=________。
(3)浓盐酸在反应KClO3+HCl―→KCl+ClO2+Cl2+()(补充完整此项化学式及化学计量数)中显示出来的性质是_。
(4)在一定条件下,PbO2与Cr3+反应,产物是Cr2O和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为________________。
(1)在反应2KMnO4+16HBr===5Br2+2MnBr2+2KBr+8H2O中,还原剂是________。
(2)已知BrFx与H2O按物质的量之比3∶5反应的产物是HF、HBrO3、Br2、O2,该反应中的氧化剂是________,还原剂是________,BrFx中的x=________。
(3)浓盐酸在反应KClO3+HCl―→KCl+ClO2+Cl2+()(补充完整此项化学式及化学计量数)中显示出来的性质是_ 。
(4)在一定条件下,PbO2与Cr3+反应,产物是Cr2O和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为________________。
(10分)高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g)  Fe(s)+CO2(g)(正反应是吸热反应),其平衡常数可表示为K = c(CO2)/c(CO),已知1100 ℃时K =0.263
Fe(s)+CO2(g)(正反应是吸热反应),其平衡常数可表示为K = c(CO2)/c(CO),已知1100 ℃时K =0.263
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比值;平衡常数K值(选填“增大”“减小”或“不变”)。
(2)1100 ℃时测得高炉中c(CO2)="0.025" mol·L-1、c(CO)="0.1" mol·L-1,在这种情况下,该反应是否处于化学平衡状态(选填“是”或“否”),此时,化学反应速率是v(正)v(逆)(选填“大于”“小于”或“等于”),其原因是。