在理论上不能用于设计原电池的化学反应是
| A.2FeCl3(aq)+2KI(aq) = 2FeCl2(aq)+2KCl(aq)+I2(aq)△H <0 |
| B.Ba(OH)2·8H2O(s)+2NH4Cl(s) = BaCl2(aq)+2NH3·H2O(aq)+8H2O(1)△H >0 |
| C.4Al(s)+ 6H2O(1)+ 3O2(g)==4Al(OH)3(s)△H <0 |
| D.Zn(s)+2MnO2(s)+2H2O(1) = 2MnOOH(s) +Zn(OH)2(s)△H <0 |
A、B两种有机物组成的混合物,当混合物质量一定时,无论A、B以何种比例混合,完全燃烧产生二氧化碳的量均相等,符合上述条件的组合是( )
①同分异构体 ②同系物 ③具有相同的实验式 ④碳的质量分数相同
A. ①②③ B. ①③④
C. ②③④ D. ①②④
在2HCHO + NaOH (浓) CH3OH +
CH3OH + 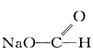 的反应中,甲醛( )
的反应中,甲醛( )
| A.仅被氧化 | B.仅被还原 |
| C.既被氧化,又被还原 | D.既未被氧化,又未被还原 |
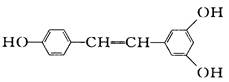 广泛存在于食物(例如桑葚、花生,尤其是葡萄)中,它可能具有抗癌性。能够跟1 mol该化合物起反应的Br2和H2的最大用量分别是( )
广泛存在于食物(例如桑葚、花生,尤其是葡萄)中,它可能具有抗癌性。能够跟1 mol该化合物起反应的Br2和H2的最大用量分别是( )
| A.1 mol、1 mol | B.3. 5 mol、7 mol |
| C.3. 5 mol、6 mol | D.6 mol、7 mol |
对于反应2H2O2 2H2O+O2↑,下列说法正确的是()
2H2O+O2↑,下列说法正确的是()
| A.H2O2是氧化剂 |
| B.O2是还原产物 |
| C.H2O2既是氧化剂,又是还原剂 |
| D.H2O是氧化产物 |
亚硝酸(HNO2)既可作氧化剂又可作还原剂,当它在反应中作氧化剂时,可能生成的产物是( )
| A.N2 | B.N2O3 | C.NH3 | D.NO2 |