A元素原子最外层电子数是次外层电子数的3倍,B元素原子次外层是最外层电子数的2倍,则关于A、B元素的判断正确的:
A.A和B元素一定都是第二周期元素 B.A和B元素一定是同一主族元素
C.B元素可以是第二周期VIA族元素 D.A和B可以相互化合形成化合物
相同物质的量的下列物质分别与等浓度的NaOH溶液反应,至体系中均无固体物质,消耗碱量最多的是()
| A.Al | B.Al(OH)3 | C.AlCl3 | D.Al2O3 |
海洋约占地球表面积的71%,对其进行开发利用的部分流程如下图所示。下列说法不正确的是( )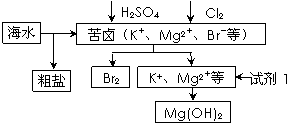
| A.可用BaCl2溶液除去粗盐中的SO42- |
| B.从苦卤中提取Br2的反应的离子方程式为:2Br- + Cl2 ="=" 2Cl- + Br2 |
| C.试剂1可以选用石灰乳 |
| D.工业上,电解熔融Mg(OH)2冶炼金属镁 |
物质的量为0.10 mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为()
| A.3.2g | B.4.0g | C.4.2g | D.4.6g |
某溶液中只含有Na+、NH4+、Ba2+、SO42-、I-、S2-中的几种,分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子是()
| A.Na+ | B.SO42- | C.Ba2+ | D.NH4+ |
如图所示,在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO4与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成。据此判断下列说法中不正确的是() 
| A.上述反应是置换反应 |
| B.上述反应是放热反应 |
| C.上述反应中CuSO4表现了还原性 |
| D.加热且无水条件下,Na可以与CuSO4反应并生成Cu |