下列变化属于吸热反应的是
①液态水汽化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释
④氯酸钾分解制氧气 ⑤生石灰与水反应生成熟石灰
| A.①④ | B.②③ | C.①④⑤ | D.②④ |
下列物质能够自身聚合成高分子化合物的是( )
| A.CH3CH2OH | B.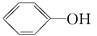 |
C.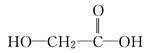 |
D.CH3COOH |
某高聚物的结构片段如下: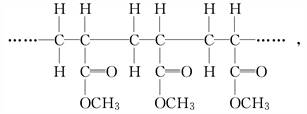
下列分析正确的是( )
| A.它是缩聚反应的产物 |
| B.其单体是CH2===CH2和HCOOCH3 |
| C.其链节是CH3CH2COOCH3 |
| D.其单体是CH2===CHCOOCH3 |
某高分子化合物的部分结构如下: 下列说法中正确的是( )
下列说法中正确的是( )
| A.若n为聚合度,则该物质的相对分子质量为97n |
B.该聚合物的链节是 |
| C.该聚合物的化学式为(C3H3Cl3)n |
| D.单体是CH2===CHCl |
生成高聚物 的单体有( )
的单体有( )
| A.1种 | B.2种 |
| C.3种 | D.4种 |
下列关于乙烯和聚乙烯的叙述中正确的是( )
| A.二者都能使溴水褪色,性质相似 |
| B.二者互为同系物 |
| C.二者最简式相同 |
| D.二者分子组成相同 |