硫代硫酸钠晶体(Na2S2O3·5H2O,式量248)俗称海波或大苏打,它易溶于水,且溶解度随温度升高而显著增大,难溶于乙醇,加热时易分解,可用于照相行业的定影剂。实验室模拟工业制备硫代硫酸钠晶体通常有以下方法,请回答有关问题。
亚硫酸钠法:Na2SO3+S+5H2O=Na2S2O3·5H2O,简易实验流程如下: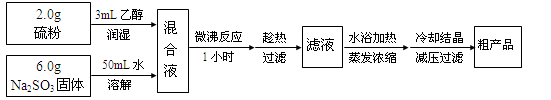
(1)硫粉用乙醇润湿的目的是 。
(2)操作中不能将溶液蒸发至干的原因是 。
(3)所得粗产品一般通过 方法提纯。
硫化碱法:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2,主要实验装置如下: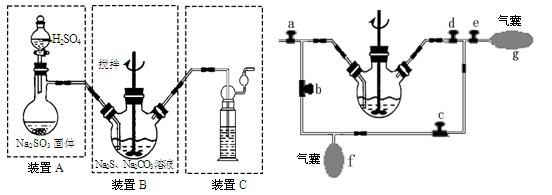
(4)装置C的作用是 。
(5)为充分利用SO2,对装置B进行改进(如上右图所示):当A中反应发生后,关闭旋塞b、e,打开a、c、d,往B中溶液通入SO2,未反应的SO2被收集到气囊f中。待f收集到较多气体时(假定此时装置A中反应已停止),关闭旋塞 ,打开旋塞 ,轻轻挤压f,使SO2缓缓地压入B中溶液再次反应,未反应的SO2又被收集在气囊g中。再将g中的气体挤压入f中,如此反复,直至完全反应。
(6)为测定硫代硫酸钠晶体粗产品的纯度。某兴趣小组称取5.0克粗产品配成250mL溶液,并用间接碘量法标定该溶液的浓度:在锥形瓶中加入25mL 0.01mol/L KIO3溶液,并加入过量的KI并酸化,发生下列反应:5I-+IO3-+6H+=3I2+3H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+S4O62-,当蓝色褪去且半分钟不变色时到达滴定终点。实验数据如下表:
| 滴定次数 |
1 |
2 |
3 |
| 消耗Na2S2O3溶液(mL) |
19.98 |
21.18 |
20.02 |
①该产品的纯度是 。
②可能造成实验结果偏低的有 (填编号)。
A.锥形瓶用蒸馏水润洗
B.滴定管未用Na2S2O3溶液润洗
C.滴定终点时俯视读数
D.若滴定前滴定管尖嘴处有气泡,滴定后消失
(16分)某中学化学研究性学习小组利用以下装置制取并探究氨气的性质。A中发生反应的化学方程式:
[实验探究]
(1)A中的反应(填“是”或“不是”)氧化还原反应。
(2)A装置还可用于制取气体(只填一种)
(3)若有10.7gNH4Cl固体,最多可制取NH3(标准状况)的体积是L
(NH4C1的摩尔质量为53.5g·mol-1)。
(4)实验室收集氨气的方法是
(5)C、D装置中颜色会发生变化的是(填“C”或“D”)
(6)当实验进行一段时间后,挤压E装置中的胶头滴管,滴人1-2滴浓盐酸,
可观察到的现象是
(7)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处
理装置,合适的装置是(填“F”或“G”)。
[知识拓展]
(8)生石灰与水反应生成Ca(OH)2并放出热量[化学方程式为CaO+H2O==Ca(OH)2]。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。你认为生石灰可用下列物质代替(填序号)。
A.碱石灰(NaOH与CaO的固体混合物) B.NaOH 固体
C.硫酸溶液 D.石灰石(含CaCO3)
[知识应用]
(9)2010 年11月9日晚,我省宁德市一冷冻厂发生氨气泄漏事件,500 多居民深夜大转移。假如你在现场,你会采用什么自救方法?
(4分)为了达到下表所列的实验目的,请选择合适的实验方法,将其标号填在相应的空格中。
实验方法:A加热 B将溶液滴在pH试纸上 C溶解、过滤、结晶 D滴加KSCN溶液
| 实验目的 |
实验方法 |
| 检验氯化亚铁是否变质 |
|
| 除去食盐中少量细沙 |
|
| 除去碳酸钠固体中少量碳酸氢钠 |
|
| 证明某地雨水样品呈酸性 |
某化学兴趣小组用铁矿石(主要成分为Fe203,还有Si02、A1203
等杂质)提取Fe2O3。操作讨程如下: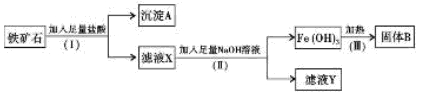
(1)(I)和(Ⅱ)步骤中分离溶液和沉淀的操作名称是;
(2)沉淀A中主要含有,固体B是;
(3)滤液Y中的阴离子除OH-、Cl-外,还有;
(4)写出(Ⅱ)步骤中生成Fe(OH)3的离子方程式
(14分) 如图所示是一个制取Cl2并以Cl2为原料进行特定反应的装置,其中各试剂瓶所装试剂为:B(Na2S)、C(FeBr2)、D(淀粉-KI)、E(SO2和BaCl2)、F(水)、H(紫色石蕊)
(1)写出实验室制取Cl2的化学方程式___________________________________________________________
(2)Ⅰ中b瓶内加入的液体是。装置Ⅰ还可用右图中的装置_______(Ⅱ或Ⅲ)代替
(3)实验开始时,先点燃A处酒精灯,打开分液漏斗旋塞和Ⅰ处活塞,让Cl2充满整个装置,再点燃G处酒精灯,回答下列问题:
①下列装置中的现象是B _________________;D_________________________
②写出E中反应的离子方程式:
_____________________________________;________________________________________
(4)G中硬质玻璃管内盛有碳粉,反应后的产物为CO2和HCl,写出G中的反应的化学方程式__________
(5)在H处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是__________________________
实验室制取乙烯的装置如下图所示,请回答: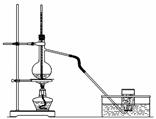
(1)实验室制取乙烯所用的乙醇为无水乙醇,但工业酒精中乙醇的含量为95%,将工业酒精转化为无
水乙醇的方法是。
(2)反应中浓硫酸起和的作用。加热前应该在烧瓶内放入少量碎瓷片,它的作用是。温度计的作用是。
(3)该实验可能产生的主要的有机副产物是。
(4)反应的化学方程式是:反应类型是。