翡翠的主要成分为NaAlSi2O6,还含有其他多种金属阳离子,其中Cr3+的含量决定其绿色的深浅。
(1)Na、Al、Si、O四种元素电负性由大到小的顺序为 。
(2)Cr3+的基态核外电子排布式为 。
(3)Cr可形成配合物K[Cr(C2O4)2(H2O)2],与H2O互为等电子体的一种分子是 (填化学式),草酸根离子(C2O42-)中碳原子的杂化方式为 ,1 mol H2C2O4分子中含有的σ键的数目为 。
(4)Cr和Ca可以形成一种具有特殊导电性的复合氧化物,晶胞如图所示。当该晶体中部分Ca2+被相同数目的La3+替代时,部分铬由+4价转变为+3价。若化合物中La3+和Ca2+的物质的量之比为 (x<0.1),三价铬与四价铬的物质的量之比为 。
(x<0.1),三价铬与四价铬的物质的量之比为 。
工业上由丙烯经下列反应可制得F、G两种高分子化合物,它们都是常用的塑料。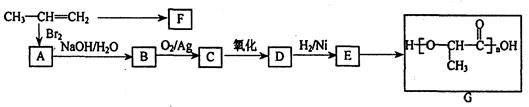
(1)聚合物F的结构简式是
(2)C与新制的Cu(OH)2共热转化为D的化学方程式是:
(3)D转化为E的化学方程式是
(4)在一定条件下,两分子E能脱去两分子水形成一种六元环状化合物,该化合物的结构简式是
四川多产五倍子,以五倍子为原料可制得化合物A,A的结构简式如右图所示: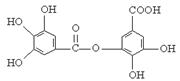
(1)1molA最多可与mol NaOH反应。
(2)A不具有的性质是(填写序号)。
①与FeCl3溶液发生显色反应②加聚反应
③与溴水发生取代反应④与碳酸氢钠溶液反应生成二氧化碳
⑤与溴水发生加成反应
(3)有机化合物B在浓硫酸催化条件下加热发生酯化反应可得到A。请写出B的结构简式
(4)有机化合物C是合成治疗禽流感药物的原料之一,C可以看成是B与氢气按物质的量之比1:2发生加成反应得到的产物。C分子中无羟基与碳碳双键直接相连的结构,它能与溴水反应使溴水褪色。请写出C与溴水反应的化学方程式:
某同学称取淀粉溶于水,测定淀粉的水解百分率。其程序如下:(共9分)
(1)各步加入的试剂为:
A,B,C。
(2)加入A溶液而不加入B溶液是否可以,其理由是。
(3)当析出1.44g砖红色沉淀时,淀粉水解率是。
1mol 某气态烃完全燃烧,生成3mol二氧化碳和2mol水,则此烃的分子式是。
一化学兴趣小组的同学通过如下实验提取海带中的碘:
①粉碎海带,加一定量的氢氧化钾溶液后高温灰化;
②用水浸泡海带灰,过滤;
③用盐酸酸化滤液,加入碘酸钾(KIO3)氧化溶液中的碘离子(I—),生成碘单质;
④用四氯化碳溶液萃取水溶液中的碘。
请回答下列问题:(共6分)
(1)实验步骤③中相关的化学反应的方程式为
(2)实验步骤③中也可用H2O2代替KIO3,相关化学反应的方程式为
。
(3)检验用四氯化碳萃取碘后的水溶液是否还有碘单质的实验方法是
。