下列关于各实验装置的叙述中,正确的是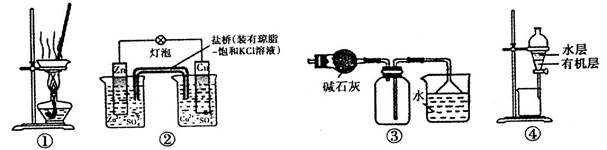
| A.装置①可用于蒸干氯化铝溶液制A1C13 |
| B.装置②盐桥中的K+自右向左移动 |
| C.装置③可用于收集NH3或HCl气体,并防止倒吸 |
| D.装置④可用于分离CCl4萃取碘水后已分层的有机层和水层 |
0.02mol·L-1的HCN溶液与0.02mol·L-1NaCN溶液等体积混合,已知混合溶液中
c(CN-)﹤c(Na+),则下列关系中,正确的是
| A.c(Na+)﹥c(CN-)﹥H+ ()﹥c(OH-) | B.c(HCN)+c(CN-)=0.04mol·L-1 |
| C.c(Na+)+c(H+)=c(CN-)+c(OH-) | D.c(CN-)﹥c(HCN) |
.能影响水的电离平衡,并使溶液中c(H+)>c(OH-)的措施是
| A.将水加热煮沸,测得pH=6 | B.向纯水中投入一小块金属钠 |
| C.向水中加入NH4Cl固体 | D.向水中加入Na2CO3固体 |
.向CH3COOH 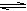 CH3COO- + H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变小的是
CH3COO- + H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变小的是
| A.H2O | B.CH3COONa | C.NH3·H2O | D.H2SO4 |
工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2+O2 2SO3,这是一个放热的可逆反应。如果反应在密闭容器中进行,下列有关说法中,错误的是
2SO3,这是一个放热的可逆反应。如果反应在密闭容器中进行,下列有关说法中,错误的是
A.使用催化剂是为了加快反应速率,提高生产效率 |
B.在上述条件下,SO2不可能100%地转化为SO3 |
C.达到平衡时,改变反应条件可以在一定程度上改变该反应的化学平衡状态 |
D.达到平衡时,SO2的浓度与SO3的浓度相等 |
一定条件下,在密闭容器中,能表示反应X(气)+2Y(气)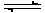 2Z(气)一定达到化学平衡状态的是
2Z(气)一定达到化学平衡状态的是
①X、Y、Z的物质的量之比为1:2:2 ②X、Y、Z的浓度不再发生变化
③密闭容器中的压强不再发生变化 ④单位时间内生成n molZ,同时生成2n mol Y
| A.①② | B.①④ | C.②③ | D.③④ |