已知:某温度时,KW=1.0×10-12。在该温度下,测得0.1mol·L-1Na2A溶液pH=6,则下列说法正确的是
A.H2A在水溶液中的电离方程式为:H2A H++HA-,HA- H++HA-,HA- H++A2- H++A2- |
| B.常温下,NH4HA溶液中滴加NaOH溶液至溶液pH=7,则c(Na+) = 2c(A2-) |
| C.相同条件下,体积相等、pH相等的盐酸与H2A溶液中和NaOH的量相等 |
| D.0.0l mol·L-l的NaHA溶液pH>2 |
联合国气候变化大会于2009年12月7~18日在哥本哈根召开。中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~45%。有效“减碳”的手段之一是节能。下列制氢方法最节能的是
A.电解水制氢:2H2O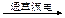 2H2↑+O2↑ 2H2↑+O2↑ |
B.高温使水分解制氢:2H2O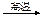 2H2↑+O2↑ 2H2↑+O2↑ |
C.太阳光催化分解水制氢:2H2O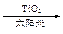 2H2↑+O2↑ 2H2↑+O2↑ |
D.天然气制氢:CH4+H2O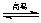 CO+3H2 CO+3H2 |
镁与100 mL 18.5 mol·L-1的浓硫酸充分反应后,镁完全溶解,同时生成气体甲 33.6L(标准状况)。将反应后的溶液稀释至1 L,测得溶液的pH=1,下列叙述不正确的是:
| A.反应中共消耗1.8 mol H2SO4 | B.气体甲中SO2与H2的体积比为4:1 |
| C.反应中共消耗36g Mg | D.反应中共转移3 mol电子 |
某有机物A是农药生产中的一种中间体,其结构简式如右图,下列叙述正确的是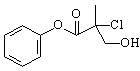
| A.有机物A属于芳香烃 |
| B.有机物A可以和Br2的CCl4溶液发生加成反应 |
| C.有机物A和浓硫酸混合加热,可以发生消去反应 |
| D.1 mol A和足量的NaOH溶液反应,最多可以消耗3 mol NaOH |
已知,常温下某浓度NaHSO3稀溶液的pH<7。则该稀溶液中下列粒子关系正确的是
| A.c(Na+)>c(HSO-3)+c(SO2-3) | B.c(Na+)>c(HSO-3)>c(H2SO3)>c(SO2-3) |
| C.c(Na+)+c(H+)=2c(SO2-3) | D.c(Na+)+c(H+)=c(HSO-3)+c(OH-) |
某无色溶液中只可能含有①Na+②Ba2+③NO-3④Cl-⑤Br-⑥SO2-3⑦SO2-4离子中的若干种(忽略水电离出的H+、OH-),依次进行下列实验,且每步所加试剂均过量,观察到的现象如下。
下列结论正确的是
| A.肯定有离子是④⑤⑥ | B.肯定没有离子是②③⑤ |
| C.可能含有的离子是①⑤⑥ | D.不能确定的例子是③④⑦ |