某学习小组推测SO2能与强氧化剂Cl2反应生成SO2Cl2,为此进行探究。
【查阅资料】SO2Cl2名称是氯化硫酰,常温下是无色液体,极易水解,遇潮湿空气会产生白雾。
【讨论】(1)SO2Cl2中S元素的化合价是 。
(2)实验中制取的SO2和Cl2在混合前都必须提纯和干燥。
【实验探究】(1)实验中制得了干燥纯净的SO2和Cl2。
(2)按下图收集满Cl2后,再通入SO2,集气瓶中立即有无色液体产生,充分反应后,将无色液体和剩余气体分离,分别对无色液体和剩余气体进行如下探究。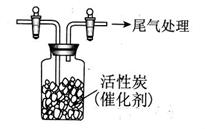
Ⅰ.探究反应产物。
向所得无色液体中加入水,立即产生白雾,振荡,静置,得无色溶液。经检验:该无色溶液中的阴离子(除OH-外)只有SO42-、Cl-。证明无色液体为SO2Cl2。
(1)SO2Cl2与水反应的化学方程式是 。
(2)验证无色溶液中含有Cl-的方法是 。
Ⅱ.探究反应进行的程度。
用NaOH溶液吸收分离出的气体,用稀盐酸酸化后,再加入BaCl2溶液,立即产生白色沉淀。
证明SO2与Cl2的反应是可逆反应。
阐述证明SO2与Cl2是可逆反应的理由 。
【质疑】有同学提出:选修四教材习题中介绍SOCl2(亚硫酰氯)常温下是无色液体,极易水解,遇潮湿空气也会产生白雾。SO2与Cl2反应若还能生成SOCl2则无法证明生成的是SO2Cl2。
SO2Cl2与水反应的化学方程式是 。
小组讨论后认为不会生成SOCl2,理由是 。
实验室要配制100 mL 2 mol/L NaCl溶液,请回答下列问题:
⑴.配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、胶头滴管、量筒和___________。
⑵.用托盘天平称取氯化钠固体,其质量为__________ g。
⑶.下列主要操作步骤的正确顺序是___________(填序号)。
①称取一定质量的氯化钠,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
⑷.如果实验过程中缺少步骤⑤,会造成所配溶液的物质的量浓度_______(填“偏高”或“偏低”或“无影响”,下同);若定容时俯视容量瓶刻度线,会造成所配溶液的物质的量浓度_________。
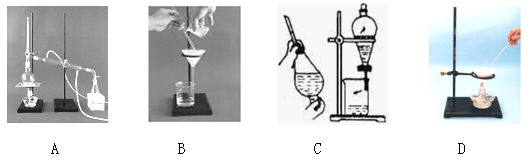
(6分)下列A、B、C、D是中学常见的混合物分离或提纯的基本装置。
|
某实验小组用如图所示装置进行铜与浓硫酸反应的实验探究。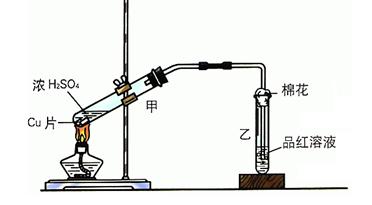
(1)写出甲中反应的化学方程式:。
(2)乙试管口的棉花应沾有的试剂是,其作用是。
(3)实验小组成员观察乙试管内液体变化是。
(4)充分反应后,若甲试管中有铜片剩余,继续向甲中加入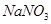 溶液,发现铜片溶解,此反应的离子方程式为。
溶液,发现铜片溶解,此反应的离子方程式为。
(5)在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是。(填字母)
| A.40.32L | B.30.24L | C.20.16L | D.13.44L |
已知某纯碱样品中含有 NaCl杂质,为测
NaCl杂质,为测 定样品中纯碱的质量分数,甲同学用下图装置及试剂进行实验(夹持仪器略)。填写下列空白处。
定样品中纯碱的质量分数,甲同学用下图装置及试剂进行实验(夹持仪器略)。填写下列空白处。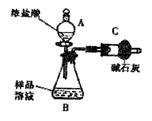
(1)仪器A、B的名称分别是、。
(2)甲同学按实验正常操作的主要步骤如下:
①;
②将ag试样放入仪器B中,加适量蒸馏水溶解,得到样品溶液;
③称量盛有碱石灰的干燥管的质量为bg;
④从仪器A中滴入浓盐酸,直到不再产生气体时为止;
⑤再次称量盛有碱石灰的干燥管的质量为cg;
(3)甲同学根据以上实验求得的样品中Na2CO3的质量分数是(用含a、b、c的式子表示)
(4)乙同学认为甲同学在实验装置设计和使用药品上都有缺陷,会导致测得的Na2CO3的质量分数偏高,而丙同学则认为甲同学的实验装置会使测得的结果偏低,丙同学认为结果偏低的原因可能是:
。
(5)若要解决乙、丙同学指出的甲同学实验中的问题,可对甲同学的实验装置和实验药品进行适当的改动,请按合理顺序选择仪器并完成下表:(用大写字母代表仪器,仪器 可重复使用,夹持仪器略)
可重复使用,夹持仪器略)
选用的 仪器 仪器 |
|||||
| 添加的药品及必要的操作 |
柴达木盆地以青藏高原“聚宝盆”之誉蜚声海内外,它有富足得令人惊讶的盐矿资源。液体矿床以钾矿为主,伴生着镁、溴等多种矿产。某研究性学习小组拟取盐湖苦卤的浓缩液(富含K+、Mg2+、Br-、SO42-、Cl-等),来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程:
请根据以上流程,回答相关问题:
(1)操作②的所需的主要仪器是
(2)参照下图溶解度曲线,得到的固体A的主要成分是(填化学式)。
(3)同学甲提出一些新的方案,对上述操作②后无色溶液进行除杂提纯,其方案如下:
【有关资料】
| 化学式 |
BaCO3 |
BaSO4 |
Ca(OH)2 |
MgCO3 |
Mg(OH)2 |
| Ksp |
8.1×10一9 |
1.08×10一10 |
1.0×10一4 |
3.5×10一5 |
1.6×10一11 |
【设计除杂过程】
a、已知试剂B是K2CO3溶液,则溶液A的主要成分是(填化学式)。
【获取纯净氯化钾】
b、对溶液B加热并不断滴加l mol· L一1的盐酸溶液,同时用pH试纸检测溶液,直至pH=5时停止加盐酸,得到溶液C。该操作的目的是。将溶液C倒入蒸发皿中,加热蒸发并用玻璃棒不断搅拌,直到出现较多晶体时,停止加热。
【问题讨论】
c、进行操作⑤中控制溶液pH=12可确保Mg2+除尽,根据提供的数据计算,此时溶液B中Mg2+物质的量浓度为。