氮气化学性质很稳定,可以通过氮的固定将空气中的氮气转化氮的化合物。氮的化合物可用于进一步合成化肥、炸药以及合成树脂等。
(1)写出氮分子的电子式______________。
(2)人工合成氨反应为N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol,在一定条件下的恒容密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是________(填序号)。
2NH3(g) △H=-92.4kJ/mol,在一定条件下的恒容密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是________(填序号)。
| A.分离出NH3 |
| B.加入催化剂 |
| C.升高温度 |
| D.增加N2的浓度 |
E.增加H2的浓度
(3)氨的接触氧化制取硝酸的过程中,900℃时,氨氧化反应阶段可能发生的反应有
| 编号 |
热化学方程式 |
平衡常数 |
| Ⅰ |
4NH3(g)+5O2(g) 4NO(g)+6H2O (g) △H1 4NO(g)+6H2O (g) △H1 |
K1=1×1053 |
| Ⅱ |
4NH3(g)+3O2(g) 2N2(g)+6H2O (g) △H2 2N2(g)+6H2O (g) △H2 |
K2=1×1065 |
| Ⅲ |
2NO(g) N2(g)+O2(g) △H3 N2(g)+O2(g) △H3 |
K3 |
反应Ⅲ的△H3=____________(用△H1、△H2表示);反应Ⅱ的平衡常数的表达式K2=__________;
该温度下K3的计算结果为__________。
(4)催化反硝法可用于治理水中硝酸盐的污染。催化反硝法中,H2能将NO3-还原为N2。25℃时,反应进行10min,溶液的pH由7变为12。反应的离子方程式为____________________________;其平均反应速率为v(NO3-)______________mol/(L•min)。
(5)实验室用下图所示装置制取NH3。若将收集NH3的试管改为集气瓶且瓶口向上排空气法收集NH3,并确保不污染环境,请画出其气体收集装置和尾气吸收装置,标出所用试剂(自选)名称。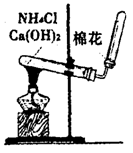
常温下,有浓度均为1 mol·L-1的下列4种溶液:
①H2SO4溶液②NaHCO3溶液③NH4Cl溶液④NaOH溶液
(1)这4种溶液pH由大到小的顺序是,其中由水电离的H+浓度最小的是。(均填序号)
(2)②中各离子浓度由大到小的顺序是,NaHCO3的水解平衡常数Kh=mol·L-1。(已知碳酸的电离常数K1=4×10-7,K2=5.6×10-11)
(3)向③中通入少量氨气,此时 的值(填“增大”、“减小”或“不变”)。
的值(填“增大”、“减小”或“不变”)。
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积④的体积(填“大于”、“小于”或“等于”之一)。
硫酸、硝酸和盐酸既是重要的化工原料也是化学实验室里必备的试剂。
(1)常温下,可用铝槽车装运浓硫酸,这是因为浓硫酸具有性;硝酸应保存在棕色试剂瓶中,这是因为硝酸具有性;敞口放置的浓盐酸浓度会减小,这是因为盐酸具有性。
(2)①在100 mL 18 mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积为13.44 L,则参加反应的铜片的质量为(选填序号);
a.115.2 g b.76.8 g c.57.6 g d.38.4 g
②若使上述①中反应剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式:。
(3)工业制盐酸是以电解饱和氯化钠溶液为基础进行的,该电解过程中阳极的电极反应式为:。
铁和铝是生产和生活中最常见的两种金属,其单质和化合物被广泛应用。
(1)硫酸铁溶液可用于浸出黄铜矿精矿,其主要反应为:
CuFeS2+4Fe3+=Cu2++5Fe2++2S(CuFeS2中S为-2价,Fe为+2价)。
关于该反应,下列说法中,正确的是(选填序号);
a.从物质分类的角度看,CuFeS2属于合金 b.反应过程中只有一种元素被还原
c.CuFeS2既作氧化剂又作还原剂 d.当转移1 mol电子时,产生16 g S
(2)高铁酸钾(K2FeO4)是一种新型水处理剂,在水中发生反应生成Fe(OH)3胶体。该反应中,高铁酸钾表现(填“氧化性”或“还原性”),Fe(OH)3胶体具有净水作用,其原因是。
(3)某同学取一张铝箔,并用针刺一些小孔,然后取一药匙过氧化钠粉末,用铝箔包好,放入右图所示装置内倒扣的漏斗中(图中铁架台和铁夹没有画出)。
按顺序写出该过程中发生反应的离子方程式:
①;
②。
化合物G是合成抗癌药物美法伦的中间体,它的结构简式为: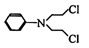
它可由中学常见的简单有机物为主要原料合成,其合成线路如下: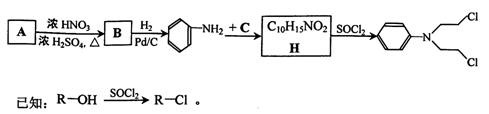
(1)D与A组成的元素相同,原子个数比也相同,按要求写出符合条件的D的结构简式:
①分子的空间构型为直线型的分子;
②分子中所有的碳原子均为sp3杂化的分子;
③NMR图谱中有5个峰,波峰面积之比为2:1:2:2:1的分子;
(2)B的一氯代物有三种同分异构体,B与足量氢气在一定条件下反应生成饱和有机物Y,则Y环上的一氯代物的同分异构体有种;
(3)已知氨气与醇在一定条件下能发生分子间的脱水反应。请写出氨气与物质C以物质的量之比为1:3反应生成的产物的结构简式,该有机物中含有的官能团的名称是,
(4)写出在加热且有浓硫酸存在条件下,H与乙二酸以物质的量比为1:1反应的化学方程式,
该反应的类型是。
(5)化合物H的一种同分异构体X,能与氯化铁溶液发生显色反应,且能与浓溴水反应,1 mol X最多消耗3 mol Br2,写出X的结构简式。(要求写出两种)
I.氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合韧是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为,该能层具有的原子轨道数为;
(2)液氨是富氢物质,是氢能的理想载体,利用 实现储氢和输氢。下列说法正确的是;
实现储氢和输氢。下列说法正确的是;
a.NH3分子中氮原子的轨道杂化方式为sp2杂化
b.NH+4与PH+4、CH4、BH-4、ClO—4互为等电子体
c.相同压强时,NH3的沸点比PH3的沸点高
d.[Cu(NH3)4]2+离子中,N原子是配位原子
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是;
II.氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示。
(1)设氯化钠晶体中Na+与跟它最近邻的Cl—之间的距离为r,则该Na+与跟它次近邻的C1—个数为,该Na+与跟它次近邻的Cl—之间的距离为;
(2)已知在氯化钠晶体中Na+的半径为以a pm,Cl—的半径为b pm,它们在晶
体中是紧密接触的,则在氯化钠晶体中离子的空间利用率为;(用含a、b的式子袁示)
(3)纳米材料的表面原子占总原子数的比例很大,这是它有许多特殊性质的原因。假设某氯化钠颗粒形状为立方体,边长为氯化钠晶胞的10倍,则该氯化钠颗粒中表面原子占总原子数的百分比为。