下图表示外界条件(温度、压强)的变化对下列反应的影响:
L(s)+G(g) 2R(g)ΔH<0。在图中,Y轴是指
2R(g)ΔH<0。在图中,Y轴是指
| A.平衡混合气中G的质量分数 | B.平衡混合气中R的质量分数 |
| C.G的转化率 | D.L的转化率 |
下列反应的离子方程式正确的是
A.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O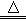 Fe(OH)3↓+3H+ Fe(OH)3↓+3H+ |
| B.用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
C.实验室用浓  盐酸与MnO2反应制Cl2:MnO2+2H++2Cl- 盐酸与MnO2反应制Cl2:MnO2+2H++2Cl-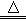 Cl2↑+Mn2++H2O Cl2↑+Mn2++H2O |
D.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu= Fe2++Cu2+ Fe2++Cu2+ |
下图有关电化学的示意图正确的是



A. B. C. D.
燃料电池是燃料(例如CO,H2,CH4等)跟氧气或空气起反应,将此反应的化学能转变为电能的装置,电解质通常是KOH溶液。下列关于甲烷燃料电池的说法不正确的是
| A.负极反应式为CH4 + 10OH-- 8 e -= CO32-+ 7H2O |
| B.正极反应式为O2 + 2H2O + 4 e -= 4OH- |
| C.随着不断放电,电解质溶液碱性不变 |
| D.甲烷燃料电池的能量利用率比甲烷燃烧的能量利用率大 |
在恒温恒容条件下,能使A(g)+B(g) C(g)+D(g)正反应速率瞬时增大的措施是
C(g)+D(g)正反应速率瞬时增大的措施是
| A.减小C或D的浓度 | B.增大D的浓度 |
| C.减小B的浓度 | D.增大A或B的浓度 |
下列反应中生成物的总能量高于反应物总能量的是
| A.碳酸钙受热分解 | B.一氧化碳燃烧 |
| C.铝与氧化铁粉末反应 | D.氧化钙溶于水 |