下列有机物的命名正确的是
A.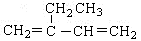 : 2—乙基—1,3—丁二烯 : 2—乙基—1,3—丁二烯 |
| B.CH3CH2CH2CH2OH:丁醇 |
C.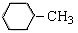 :甲苯 :甲苯 |
| D.HOCH2CH2CH2OH: 1,3-二丙醇 |
沼气是一种能源,它的主要成分是CH4,0.5molCH4完全燃烧生成CO2和液态水时放出445kJ的热量,则下列热化学方程式中正确的是
| A.2CH4(g)+4O2(g)=2CO2(g)+4H2O(g)△H=+890kJ•mol﹣1 |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=+890kJ•mol﹣1 |
| C.1/2 CH4(g)+O2(g)=CO2(g)+H2O(l)△H=﹣890kJ•mol﹣1 |
| D.CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=﹣890kJ•mol﹣1 |
在2A+B  3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是
A.v(A)=0.5 mol·L-1·s-1
B.v(B)=0.3 mol·L-1·s-1
C.v(C)=0.8 mol·L-1·s-1
D.v(D)=1.6 mol·L-1·min-1
下列说法或表示正确的是
| A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.物质发生化学变化时一定伴随着放热现象 |
| C.稀溶液中:H+(aq)+OH﹣(aq)=H2O(l);△H=﹣57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含l mol NaOH的溶液混合,放出的热量大于57.3kJ |
| D.在25℃101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ的热量,则H2燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l);△H=﹣285.8kJ/mol |
对可逆反应4NH3(g) + 5O2(g)  4NO(g) + 6H2O(g),下列叙述正确的是
4NO(g) + 6H2O(g),下列叙述正确的是
| A.化学反应速率关系是:2υ正(NH3) = 3υ正(H2O) |
| B.达到化学平衡时,4υ正(O2) = 5υ逆(NO) |
| C.达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大 |
| D.若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态 |
下列变化过程中ΔH<0的是
| A.Na与水反应 |
| B.HCl分解为H2和Cl2 |
| C.电解Al2O3得到Al和O2 |
| D.Ba(OH)2·8H2O与NH4Cl晶体混合反应 |