如图,a和b均为金属棒,当电流计中指针发生偏转,下列说法正确的是
| A.电极a表面一定呈红色 |
| B.电极b作负极 |
| C.电极a或b其中有一极一定是金属铁 |
| D.该装置能量转化形式为化学能转化为电能 |
硫酸的产量是衡量一个国家化工水平的标志。2SO2(g) + O2(g)  2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。
2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。
| 甲 |
乙 |
丙 |
||
| 起始物质的量 |
n(SO2) / mol |
0.4 |
0.4 |
0.8 |
| n(O2) / mol |
0.24 |
0.48 |
0.48 |
|
| SO2的平衡转化率 |
80% |
α1 |
α2 |
下列判断中,正确的是
A.甲中反应的平衡常数大于乙
B.平衡时,SO2的转化率:α1<80%<α2
C.该温度下,乙中平衡常数值为400
D.平衡时,丙中c(SO3)是甲中的2倍
某原电池装置如图所示,电池总反应为2Ag+Cl2 2AgCl。下列说法正确的是
2AgCl。下列说法正确的是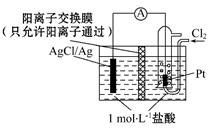
A.正极反应为AgCl+e- Ag+Cl- Ag+Cl- |
| B.放电时,交换膜左侧溶液中有大量白色沉淀生成 |
| C.若用NaCl溶液代替盐酸,则电池总反应随之改变 |
| D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.01 mol离子 |
X、Y、Z、W的原子序数依次增大的短周期元素,其含氧酸根离子不能破坏水的电离平衡的是
| A.XO32- | B.ZO42- | C.YO2- | D.WO— |
在实验室中常以草酸钠(Na2C2O4)为标准液,通过氧化还原滴定来测定高锰酸钾溶液的浓度,其反应的化学方程式为:C2O42—+MnO4—+H+—→Mn2++CO2↑+H2O。下列有关草酸钠滴定高锰酸钾实验的叙述,正确的是
| A.滴定过程中,高锰酸钾被氧化,草酸钠被还原 |
| B.用酸式滴定管量取草酸钠溶液 |
| C.该反应中,消耗的草酸钠与高锰酸钾的物质的量之比为5:2 |
| D.为便于滴定终点的判断,滴定时必须往体系中加入指示剂 |
下列实验“操作和现象”与“结论”对应关系正确的是
| 操作和现象 |
结论 |
|
| A |
向装有 溶液的试管中加入稀 溶液的试管中加入稀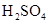 ,在管口观察到红棕色气体 ,在管口观察到红棕色气体 |
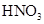 分解成了 分解成了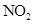 |
| B |
向淀粉溶液中加入稀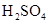 ,加热几分钟,冷却后再加入新制 ,加热几分钟,冷却后再加入新制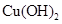 浊液,加热,没有红色沉淀生成 浊液,加热,没有红色沉淀生成 |
淀粉没有水解成葡萄糖 |
| C |
向无水乙醇中加入浓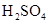 ,加热至170℃,产生的气体通入酸性 ,加热至170℃,产生的气体通入酸性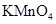 溶液,紫红色褪去 溶液,紫红色褪去 |
使溶液褪色的气体只是乙烯 |
| D |
向饱和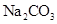 中通入足量CO2,溶液变浑浊 中通入足量CO2,溶液变浑浊 |
析出了NaHCO3 |