以下反应最符合绿色化学原子经济性要求的是
| A.乙烯聚合为聚乙烯高分子材料 | B.甲烷与氯气制备一氯甲烷 |
| C.以铜和浓硝酸为原料生产硝酸铜 | D.用SiO2制备高纯硅 |
下列分子或离子中,含有孤对电子的是()
| A.H2O | B.CH4 | C.SiH4 | D.NH4+ |
下列表示式错误的是( )
A.Na+的电子排布图: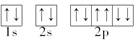 |
B.Na+的结构示意图: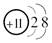 |
| C.Na的电子排布式:1s22s22p63s1 |
| D.Na的简化电子排布式:[Ne]3s1 |
把一定量的Na2O2和NaHCO3混合粉末分为两等份,将其中一份加入到100mL稀盐酸中恰好完全反应,生成干燥的气体2.24L(标准状况),再将此气体通入到另一份混合物中,充分反应后,气体减少为2.016L(标准状况),则原混合粉末中Na2O2和NaHCO3的物质的量之比及原稀盐酸的物质的量浓度可能是( )
| A |
B |
C |
D |
|
| Na2O2和NaHCO3的物质的量之比 |
8:1 |
9:2 |
1:8 |
2:9 |
| 原稀盐酸的物质的量浓度(mol/L) |
3.4 |
1.1 |
1.8 |
1.3 |
下图所示的实验,能达到实验目的的是…………………………………() 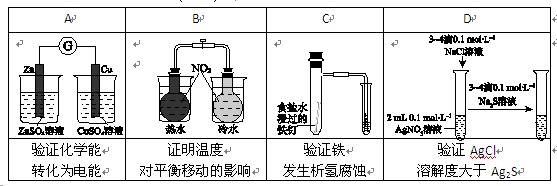
某二元酸(化学式H2A)在水中的电离方程式是H2A→ H+ + HA-、HA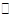 H++A2-又知0.1 mol/LNaHA溶液的pH = 2。则下列说法不正确的是…………………( )
H++A2-又知0.1 mol/LNaHA溶液的pH = 2。则下列说法不正确的是…………………( )
A、因为A2-+H2O 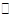 HA-+OH-,所以Na2A溶液显碱性
HA-+OH-,所以Na2A溶液显碱性
B、0.1 mol/L H2A溶液中氢离子的物质的量浓度为0.11 mol/L
C、NaHA溶液中各种离子浓度的关系是c(Na+) > c(HA-) > c(H+) > c(A2-) > c(OH- )
D、在NaHA溶液中,HA-电离的趋势大于其水解的趋势