有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
| 实 验 步 骤 |
解 释 或 实 验 结 论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍。 |
试通过计算填空: (1)A的相对分子质量为: 。 |
| (2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g。 |
(2)A的分子式为: 。 |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况)。 |
(3)用结构简式表示A中含有的官能团: ___________。 |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况)。 |
(3)用结构简式表示A中含有的官能团:____________。 |
(4)A的核磁共振氢谱如下图: |
(4)A中含有______种氢原子。 |
| (5)综上所述,A的结构简式 。 |
(I)由Zn、Fe、Cu、Ag四种金属按下表中装置进行实验,根据实验现象填表:
装 置 |
 |
 |
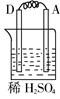 |
| 现象 |
金属A不断溶解 |
C的质量增加 |
A上有气体产生 |
| 正极反应式 |
(II)碘是人体必须的元素之一,海洋植物如海带、海藻中含有丰富的以碘离子形式存在的碘元素。海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验: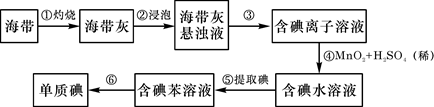
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器及用品是
(填字母编号)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.玻璃棒 G .石棉网
(2)步骤③的实验操作名称是;步骤⑤实验操作名称是。
(3)步骤④也可以用(填试剂名称)来起相同作用,写出该反应的离子方程式。
(4)步骤⑤中,除选择用苯来提取碘,还可选择的试剂是_______________。
A.酒精B.醋酸 C. 四氯化碳D. 甘油 E.己烷 F.直馏汽油
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:。
实验室用二氧化锰和浓盐酸制取氯气
(1)实验室制取氯气的离子方程式
(2)二氧化锰放在浓盐酸放在(填仪器名称)
(3)实验室制取氯气以前,首先应该进行除了向上排气法收集氯气外,还可以用收集。
(4)图中两个洗气瓶放置的试液依次是,图中错误是
(5)碱石灰的作用是
(6)制取标准状况下11.2L氯气转移电子摩尔,被氧化的氯化氢是摩尔。
用铜片、锌片和稀硫酸及若干其他器材组合成一个原电池,画出装置图并回答 (1)画出装置图。
(2)从理论上讲,预期看到的现象是
(3)实验过程中,观察到锌片上有少量气泡冒出,铜片上有大量气泡冒出。试解释:。
(4)此电池的负极是,正极的电极反应式是。
(5)该电池工作一段时间,将两个电极小心取出洗涤并晾干,经称量发现锌片比原来减少3.25 g。请计算理论上导线中共通过了mol电子
某校化学学习小组拟验证NO能被氨气还原并测定其转化率,设计如下实验:
参考知识:NO气体 与FeSO4溶液反应生成可溶性硫酸亚硝基合铁(Ⅱ):NO+FeSO4=Fe(NO)SO4
与FeSO4溶液反应生成可溶性硫酸亚硝基合铁(Ⅱ):NO+FeSO4=Fe(NO)SO4
试回答下列问题:
⑴实验室用氯化铵与氢氧化钙固体制备氨气,应选用的装置是
该反应的化学方程式
实验室通常用法收集氨气,检验该气体是否收集满方法
⑵装置③、④若用同一装置,则该装置中所盛装的药品是
| A.Na2O2 | B.浓硫酸 | C.P2O5 | D.碱石灰 |
⑶装置⑥中,粗玻璃管X的作用,装置⑦的作用
⑷装置⑥的广口瓶中,除生成Fe(NO)SO4外,还有白色沉淀生成,写出生成该沉淀的离子方程式
⑸若参加反应的NO为2.688L(标准状况,下同),氨气过量,最后收集到2.016LN2,则装置⑤中NO的转化率为
三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物。探究过程如下:
查阅资料:Cu2O是一种碱性氧化物, 溶于稀硫酸生成Cu和CuSO4, 在空气中加热生成CuO
提出假设
假设1:红色粉末是Fe2O3假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂。
⑴若假设1成立,则实验现象是。
⑵若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁。你认为这种说法合理吗?,简述你的理由(不需写出反应的方程式 )
⑶若固体粉末完全溶解, 向所得溶液中滴加 KSCN 试剂时溶液不变红色 , 则证明原固体粉末是,写出实验过程中发生的氧化还原反应的离子方程式
探究延伸:若经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物。
⑷实验小组欲用加热法测定Cu2O的质量分数。取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b > a),则混合物中Cu2O的质量分数为。
⑸某铝土矿样品经测定是由Al2O3、Fe2O3、 FeO、 SiO2等氧化物组成,取样品适量放入烧杯中,加入稀硫酸将其溶解,过滤,取滤液少量于试管中,若证明滤液中含有+2价的铁,选用的试剂和现象为.