科学家发明的透明坚硬镁铝氧化物新型材料,可以用作显示器和手机屏幕。下列有关镁和铝的说法正确的是
| A.镁的金属性比铝弱 |
| B.镁和铝的氧化物都可以与盐酸反应 |
| C.镁和铝原子的最外层电子数都为3 |
| D.镁和铝的氧化物都可以与氢氧化钠溶液反应 |
用纯净的CaCO3与稀盐酸反应制取CO2,实验过程记录如图所示。根据分析、判断,正确的是 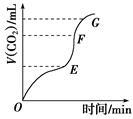
| A.OE段表示反应速率最快 |
| B.EF段表示反应速率最快,单位时间内收集的CO2最多 |
| C.FG段表示收集的CO2最多 |
| D.OG段表示随着时间的推移,反应速率逐渐增快 |
在2 L容器中发生3A+B  2C的反应,最初加入的A、B都是4 mol,若10 s 后反应达到平衡,测得A的平均反应速率为0.15 mol·L-1·s-1,则10 s后容器内B的物质的量为
2C的反应,最初加入的A、B都是4 mol,若10 s 后反应达到平衡,测得A的平均反应速率为0.15 mol·L-1·s-1,则10 s后容器内B的物质的量为
A.1.5 molB.1.0 mol C.3.0 molD.2.4 mol
观察下列几个装置示意图,有关叙述正确的是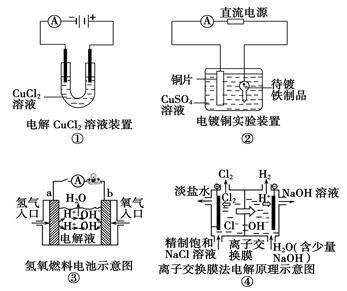
| A.装置①中阳极上析出红色固体 |
| B.装置②的待镀铁制品应与电源正极相连 |
| C.装置③中外电路电子由a极流向b极 |
| D.装置④中的离子交换膜允许阳离子、阴离子、水分子自由通过 |
某课外研究小组的同学将FeCl3(aq)滴加到5%H2O2溶液后,发现产生无色气体由慢到快,最后再变慢;溶液温度升高;同时溶液颜色由黄色立即变为棕褐色,当反应殆尽时,溶液又恢复黄色,由此得出以下结论,你认为错误的是
| A.H2O2的分解反应为放热反应 |
| B.FeCl3是H2O2分解反应的催化剂 |
| C.与不加FeCl3(aq)相比,当H2O2均完全分解时,加FeCl3(aq)使反应放出的热量更多 |
| D.将少量FeCl2溶液滴入过量5%H2O2溶液中,则除溶液颜色变化不同外,其它现象相同 |
按图甲装置进行实验,若图乙中横坐标x表示通过电极的电子的物质的量。下列叙述正确的是
| A.F表示反应生成Cu的物质的量 |
| B.E表示反应生成O2的物质的量 |
| C.E表示反应实际消耗H2O的物质的量 |
| D.F表示反应生成H2SO4的物质的量 |