用容量瓶准确配制一定浓度的NaCl溶液时,下列操作会使溶液浓度偏高的是
| A.用粗盐代替NaCl固体 |
| B.定容时,溶液液面低于容量瓶刻度线 |
| C.从烧杯向容量瓶转移溶液时,有少量溶液溅出 |
| D.向容量瓶转移溶液时,容量瓶中有少量蒸馏水 |
当光束通过下列分散系时,能观察到丁达尔效应的是
| A.蔗糖溶液 | B.盐酸 | C.氯化钠溶液 | D.Fe (OH)3 胶体 |
下列物质中,属于电解质的是
| A.CO2 | B.H2 | C.Na2SO4 | D.Cu |
有一种气体的质量为14.2g,体积是4.48L(标准状况),该气体的摩尔质量是
| A.71 g·mol-1 | B.71 | C.28.4g·mol-1 | D.28.4 |
下列说法正确的是()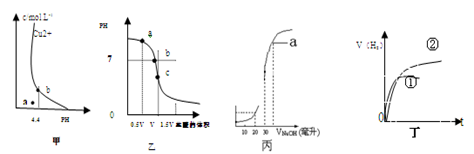
A.图甲表示某温度下,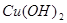 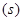 在溶液中达到沉淀溶解平衡后,改变溶液PH, 在溶液中达到沉淀溶解平衡后,改变溶液PH,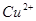 浓度的变化。由图可知 浓度的变化。由图可知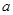 点溶液未达到饱和,因此, 点溶液未达到饱和,因此,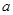 点的 点的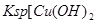 ]小于 ]小于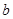 点。 点。 |
B.图乙表示在室温时用一定浓度的盐酸滴定V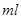 同浓度的氨水。 同浓度的氨水。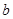 点时溶液中 点时溶液中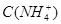 = =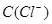 ,且溶液中水的电离程度最大。 ,且溶液中水的电离程度最大。 |
C.图丙表示在室温时,用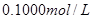 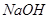 溶液滴定30.00ml0.1mol/L 溶液滴定30.00ml0.1mol/L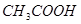 溶液,点a所示溶液中C( 溶液,点a所示溶液中C( > >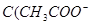 )> )>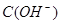 > >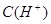 |
D.图丁可表示同体积同PH的某一元强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发生反应生成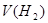 随时间( 随时间(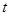 )的变化情况。 )的变化情况。 |
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是元素周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期, R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是()
| A.元素Y、Z、W的离子具有相同电子层结构,其半径依次增大 |
B.元素X不能与元素Y形成化合物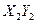 |
| C.元素Y、R分别与元素X形成的化合物的热稳定性:XMY>XMR |
| D.元素W、R的最高价氧化物对应的水化物都是强酸 |