已知下表所示数据:
| 物质 |
熔点(℃) |
沸点(℃) |
密度(g·cm-3) |
| 乙醇 |
-117.3 |
78.5 |
0.79 |
| 乙酸 |
16.6 |
117.9 |
1.05 |
| 乙酸乙酯 |
-83.6 |
77.5 |
0.90 |
| 浓硫酸 |
|
338.0 |
1.84 |
某学生实验室制取乙酸乙酯的主要步骤如下:
①在30 mL的大试管A中按体积比2∶3∶3配制浓硫酸、乙醇和乙酸的混合溶液。
②按图甲连接好装置(装置气密性良好),用小火均匀加热装有混合液的大试管 5~ 10 min。
③待试管B收集到一定量产物后停止加热,撤出试管B并用力振荡,然后静置待分层。
④分离出乙酸乙酯层,洗涤、干燥。
请根据题目要求回答下列问题:
(1)配制该混合液的主要操作步骤为_______________________________________。
(2)导管不能插入到Na2CO3溶液中的原因是_________________________。
(3)步骤②中需要小火均匀加热,其主要原因是__________________________________。
(4)指出步骤③所观察到的现象:____________________________________________。
(5)充分振荡试管,然后静置,待液体分层后,分液得到的上层液体即为乙酸乙酯。分离出乙酸乙酯层后,可以用用________________________洗涤。
A.乙醇 B.饱和食盐水 C.碳酸钠溶液 D.NaOH溶液
为了验证碱金属元素和第三周期金属元素金属性的相对强弱,某课外活动小组的同学设计如下实验,请根据要求回答下列问题:
(1)取少量金属钠和金属钾分别放入盛的烧杯中,观察到钾的现象是;由此得出的结论是。
(2)将镁条打磨至银白色后放入盛有上述物质的试管中,明显现象(填“有”或“没有”),后(填操作名称)可观察到有大量气泡产生,反应的化学方程式是;
(3)将打磨好的镁条和铝条分别放入盛的试管中,观察到明显的现象,铝条反应的离子方程式是,由(1)(2)(3)可得出的结论是;
(4)某同学在学习了电化学基础知识后,设计了如图所示(X、Y分别是Mg、Al)的装置进行实验,发生氧化反应的负极金属性强,但发现镁条上有气体产生,由此得出了与实验(3)相反的结论,你知道这位同学所用的Z溶液是,其负极的电极反应式是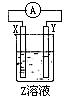
某同学为了验证Fe3+是否能氧化H2SO3生成了SO42–,他用50mL0.1mol/LFeCl3溶液吸收制取SO2气体的尾气,进行以下实验:
(1)检验吸收液中的SO42–: __________
_____________________________________________,证明Fe3+能够把H2SO3氧化成SO42–。
(2)请配平并完成上述反应中的化学方程式:
2FeCl3+SO2+==2FeCl2+H2SO4+2HCl,反应中的还原剂是 _____ (写化学式)。
(3)吸收液中除了含有H+、Cl–、SO42–以外,对其它成份(Fe3+、Fe2+、H2SO3)的可能组合进行探究:
①提出假设。
假设1:溶液中存 在Fe3+、Fe2+;
在Fe3+、Fe2+;
假设2:溶液中存在;
假设3:溶液中存在Fe2+ 而不存在H2SO3(二者恰好完全反应)。
②设计方案、进行实验,验证假设。请在表中写出实验步骤以及预期现象和结论(可以不填满)。限选实验试剂和仪器:试管、滴管、0.1moL L-1KMnO4、0.1moL
L-1KMnO4、0.1moL L-1KSCN溶液、品红
L-1KSCN溶液、品红 稀溶液。
稀溶液。
| 实验步骤 |
预期现象和结论 |
| 步骤1:用试管取样品溶液2-3mL,再用滴管取 |
若出现血红色,则假设1成立;若未出现血红色,则假设2或假设3成立。 |
| 步骤2: |
结合步骤1的现象和结论, ________________________________________. |
某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯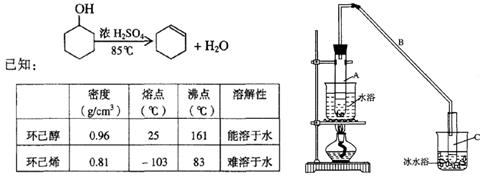
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是,导管B除了导气外还具有的作用是。
②试管C置于冰水浴中的目的是。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在层(填上或下),分液后用_________(填入编号,单选)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3 溶液
溶液
②再将环己烯按下图装置蒸馏,冷却水从_________口进入,目的是_____________________________。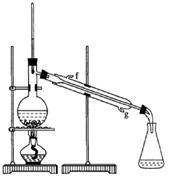
③收集产品时,控制的温度应在_________左右 ,实验制得的环己烯精品质量低于理论产量,可能的原因是(单选)
,实验制得的环己烯精品质量低于理论产量,可能的原因是(单选)
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
用图示装置制取PCl3,在E中放入足量白磷,将氯气不间断地通入E,氯气与白磷就会发生反应,并放出热量(温度高于75℃)。已知:PCl3和PCl5遇水强烈反应,它们熔沸点数据如下: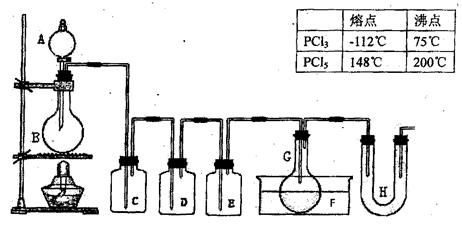
请根据图中装置回答下列问题:
(1)检查该装置气密性的方法是。
(2)为得到氯气,若B中加入MnO2,则A中应加入 ,发生反应的化学方程式为。
,发生反应的化学方程式为。
(3)若发现C中气泡产生过猛,需要进行的操作的关键是。
(4)在反应开始时主要生成PCl3,而后来主要生成PCl5,原因可能是;从PCl3和PCl5的混合物中分离也PCl3的最佳方法是(选填序号)。
a.蒸馏 b.分液 c.升华
(5)生成的PCl3在G中收集,则F中盛有,作用是
(6)C、D、H所盛的试剂分别是:C;D ;H。
;H。
(7)如果E中反应放热较多,G处的导管可能发生堵塞,其原因 是。
是。
(1)写出实验室由苯和浓硝酸反应制取硝基苯的化学方程式:.
该反应属于反应。
(2)如图所示的实验装置图中存在哪些错误?请指正。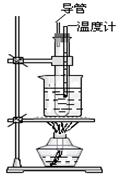
①;
②;
③。
(3)在试管中将两种浓酸混和的操作方法是
(4)试简述水浴加热的优点。