如图是硫酸试剂瓶标签上的部分内容。现实验室需要240ml 4.6mol/L的稀硫酸用该硫酸配置,
则:(1)需要该浓硫酸的体积为 mL;
(2)可供选用的仪器有:胶头滴管;烧瓶;烧杯;药匙;量筒;托盘天平.配置稀硫酸时,还缺少的仪器有______、______。
(3)配置过程中有几个关键的步骤和操作如图所示:将下列实验步骤A-F按实验过程先后次序排列_______________。
(4)该同学实际配置得到的浓度为4.5mol/L,可能的原因是 。
| A.量取浓H2SO4时俯视刻度 |
| B.容量瓶洗净后未经干燥处理 |
| C.将稀释后的稀硫酸立即转入容量瓶后,紧接着就进行以后的实验操作 |
| D.定容时仰视刻度线 |
Ⅰ.有学生用五氧化二磷作为乙醇脱水制乙烯的催化剂,进行相关实验。按如表所示的量和反应条件在三颈瓶中加入一定量P2O5,再注入95%的乙醇,并加热,观察现象。
| 实验 |
P2O5/g |
95%乙醇量/mL |
加热方式 |
| 实验1 |
2 |
4 |
酒精灯 |
| 实验2 |
2 |
4 |
水浴70 |
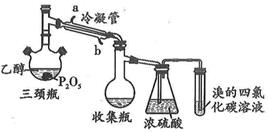
实验结果如下:
| 实验 |
实验现象 |
||
| 三颈瓶 |
收集瓶 |
试管 |
|
| 实验1 |
酒精加入时,立刻产生白雾,当用酒精灯加热时,有气泡产生,并逐渐沸腾,生成黏稠状液体 |
有无色液体 |
溶液褪色 |
| 实验2 |
酒精加入时,立刻产生白雾,当用水浴加热时,不产生气泡,一段时间后,反应瓶内生成黏稠状液体 |
有无色液体 |
溶液不褪色 |
根据上述材料,完成下列填空。
写出实验室用乙醇制乙烯的化学方程式:。
(2)上图装置中冷凝管的作用是。
(3)实验1使溴的四氯化碳溶液褪色的物质是(写结构简式)
(4)根据实验1、2可以推断:
①以P2O5作为催化剂获得乙烯的反应条件是。
②P2O5与95%乙醇在水浴70℃加热条件下(三颈瓶、收集瓶中的液体经检验为磷酸三乙酯)可以发生的有机反应的类型是反应。
II.下图所示装置工作时均与H2有关。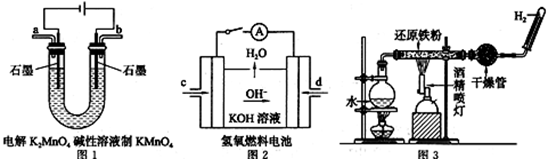
①图1所示装置中阳极的电极反应式为。
②图2所示装置中,通入H2一极的电极反应式为。
③某同学按图3所示装置进行实验,实验结束后,将玻璃管内固体物质冷却后,溶于稀硫酸,充分反应后,滴加KSCN溶液,溶液不变红,再滴入新制氯水,溶液变为红色。该同学据此得出结论:铁与水蒸气反应生成FeO和H2。该结论(填“严密”或“不严密”),你的理由是(用离子方程式表示)。
(16分)氨水是一种的常用的化学试剂。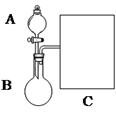
(1)以浓氨水和生石灰为原料,用如下装置为发生装置,可制取少量氨气。已知:NH3·H2O+CaO=Ca(OH)2+NH3↑。
①生石灰应该装在____(填A或B)。
②试从电离平衡角度分析该实验中氨气逸出的原因:
③现要用试管和必要实验用品收集一试管氨气,请在C处补充相应收集装置。
(2)化学兴趣小组用氨水与硝酸银溶液配制好银氨溶液后,进行乙醛的银镜反应实验,但部分同学实验时间长,且效果不明显。影响乙醛银镜反应速率的因素有哪些呢?请你完成如下猜想:
①猜想:因素一:银氨溶液的pH大小;因素二:____________________ 。
②你设计实验验证上述“因素一”,完成下表中内容。
提供试剂:乙醛、2%稀氨水、 0.25mol/L NaOH溶液、盐酸 、 2% AgNO3溶液
实验用品:烧杯(装有热水)、试管
| 实验步骤 |
实验操作 |
预期现象及结论 (步骤1只写现象) |
| 1 |
在A、B两支洁净的试管中各加入1mL 2%的AgNO3溶液,然后,此时制得pH均约为8的银氨溶液。 |
|
| 2 |
往A、B试管加入3滴乙醛,然后在A试管中加;振荡后将两支试管放在热水浴中温热。 |
若A试管比B试管出现的银镜时间短、光亮,则 若A试管比B试管出现的银镜时间长,则 |
炼锌厂产生的工业废渣——锌渣(除了含Zn外,还含有Fe、Al、Cd和SiO2等杂质),利用锌渣制取并回收ZnSO4·7H2O和金属镉是一个有益的尝试,其流程如下:
已知:Fe3+、Al3+、Zn2+、Cd2+、Fe2+以氢氧化物完全沉淀时的pH分别为:3.2,4.7,6.5,9.4,9.7;锌的金属活动性比镉强。
试回答下列问题:
(1)“浸出”时用到的“试剂X”为(填名称)。
(2)写出“氧化”过程的离子方程式。
(3)“调pH”过程可以选用。(从以下选项选择,填序号)
A.H2SO4B.ZnOC.NaOH
“滤渣2”的主要成分是(填化学式,下同)。
(4)“试剂Y”是___________
(5)“操作1”是;在“操作1”时,必须采取的实验措施是。
(10分)对叔丁基苯酚( )工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚。
)工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚。
实验步骤如下: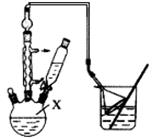
步骤l:组装仪器,用量筒量取2.2 mL叔丁基氯(过量),称取1.6 g苯酚,搅拌使苯酚完全溶解,并装入滴液漏斗。
步骤2:向X中加入少量无水AlCl3固体作催化剂,打开滴液漏斗旋塞,迅速有气体放出。
步骤3:反应缓和后,向X中加入8 mL水和1 mL浓盐酸,即有白色固体析出。
步骤4:抽滤得到白色固体,洗涤,得到粗产物,用石油醚重结晶,得对叔丁基苯酚1.8 g。
(1)仪器X的名称为。
(2)步骤2中发生主要反应的化学方程式为 _________________________。
(3)图中倒扣漏斗的作用是。苯酚有腐蚀性,若其溶液沾到皮肤上可用洗涤。
(4)下列仪器在使用前必须检查是否漏液的是(填选项字母)。
| A.量筒 |
| B.容量瓶 |
| C.滴定管 |
| D.分液漏斗 |
E.长颈漏斗
(5)本实验中,对叔丁基苯酚的产率为。(请保留三位有效数字)
(14分)某化学兴趣小组为了探究AgNO3的性质,通过查阅资料和老师指导设计了如下实验:
Ⅰ.探究AgNO3的氧化性
实验方法:将光亮的铁丝伸入新配制的AgNO3溶液中,一段时间后将铁丝取出。为检验溶液中Fe的氧化产物,先将溶液中的Ag除尽后,进行了如下实验。可选用的试剂:蒸馏水、稀氨水、KSCN溶液、高锰酸钾酸性溶液、新制氯水。
(1)请完成下表:
| 实验操作 |
现象 |
结论 |
| 取少量除尽Ag+后的溶液于试管中,____________________,充分振荡 |
_____________________ _____________________ |
存在Fe3+ |
| 取少量除尽Ag+后的溶液于试管中,____________________,充分振荡 |
_____________________ _____________________ |
不存在Fe2+ |
【实验结论】Fe的氧化产物为Fe3+。
Ⅱ.探究AgNO3的热稳定性
用下图所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体。
当反应结束后,试管中残留同体为黑色。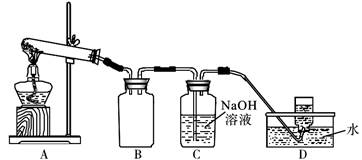
(2)装置B的作用是________________________。
(3)经小组讨论并验证该无色气体为O2,其验证方法是___________________________________。
(4)【查阅资料】Ag2O和粉末状的Ag均为黑色;Ag2O可溶于氨水和稀硝酸。
【提出设想】试管中残留的黑色同体可能是:i.Ag;ii.Ag2O;iii.__________________。
【实验验证】该小组为验证上述设想iii是否成立,进行了如下实验(仪器和药品任选)
| 实验操作 |
现象和结论 |
【实验结论】若假设i成立,该小组得出AgNO3固体热分解反应的化学方程式为______________。