塑料电镀是近几十年来发展起来的表面处理新技术,广泛用于电子、家用电器、汽车、建筑等工业。它先是在塑料、陶瓷等非金属表面采用化学沉积的方法沉积出一层金属层,再用电解的方法镀上铜层,电解液为 CuSO4水溶液。
(1)请写出电解时,阴极上可能发生的反应:
① ;② 。
(2)设通过0.01mol电子后,阴极上沉积出铜 0.2879g , 阴极上还可能放出的气体是 。计算标准状况下阴阳极共放出气体的体积 。
A、B、C、D、E是位于短周期的主族元素。已知:①热稳定性:HmD>HmC;②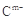 、
、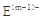 具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
(1)HmDm的电子式___________________。
(2)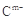 、
、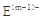 的还原性强弱顺序为:_________,能证明其还原性强弱的离子方程式为______。
的还原性强弱顺序为:_________,能证明其还原性强弱的离子方程式为______。
(3)将E的单质通入A与D形成的化合物的水溶液中,其离子方程式为:_____________________。
(4)常温下,将等物质的量浓度的HmC溶液和A的最高价氧化物对应的水化物溶液等体积混合,写出该反应的离子方程式。在该溶液中溶质中含有的化学键类型是。
(5)在A、B、C、E单质中,符合下列转化关系的是_____________(填元素符号)。
下表是元素周期表的一部分,按要求回答下列有关问题:
 |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
O |
| 2 |
① |
② |
||||||
| 3 |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
|
| 4 |
⑩ |
⑪ |
⑫ |
(1)在这些元素中,最活泼的金属元素是_____(填写元素符号,下同);最活泼的非金属元素是_______;最不活泼的元素是________。
(2)画出⑥原子的结构示意图________;⑩离子结构示意图________。
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是________;(填写物质的化学式,下同)碱性最强的是________;呈两性的氢氧化物是________。
(4)画出④和⑧形成的化合物的电子式。
(5)在③与④中,化学性质较活泼的是________,怎样用化学实验证明:________。
现有如下两个反应:
A.NaOH + HCl=NaCl + H2O
B.2FeCl3+Cu=2FeCl2+CuCl2
(1)根据两反应本质, 判断能否设计成原电池:A。_______, B。________(选择“能”或“不能”);
(2)如果不能, 说明其原因_____________________________________;
(3)如果可以, 则写出正、负极材料及其电极反应式, 电解质溶液名称:
负极材料________,电极反应式_______________,电解质溶液名称____________,
正极材料________,电极反应式_______________。
(10分)(1)请选择合适方法的字母代号填空:
①从海水中提取粗盐________;② 煤转化为焦炭、煤焦油等________;
③ 工业上由氧化铝制取金属铝________;④ 提纯氢氧化铁胶体________。
A.过滤 B.裂解 C.分馏 D.裂化 E.干馏 F.还原
G.电解 H.溶解 I.渗析 J.蒸发 K.氧化
(2)某可逆反应从0—2分钟进行过程中, 在不同反应时间各物质的量的变化情况如右图所示。则该反应的的反应物是,生成物是,此反应(填是或不是)可逆反应;反应开始至2分钟时, _____(能或不能)用C表示反应速率,2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了 ____状态,此时正反应速率逆反应速率(填等于或不等于)。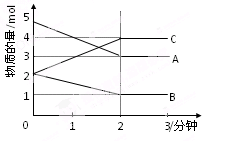
已知:①R—C≡N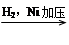 RCH2NH2
RCH2NH2
②R—CN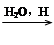 RCOOH,
RCOOH,
③R—Cl+CN- R—CN+Cl-(R为烃基)。
R—CN+Cl-(R为烃基)。
玉米芯、甘蔗渣等废物水解发酵后可制得糠醛 ,它是重要的化工原料,它在一定条件下可发生以下变化:
,它是重要的化工原料,它在一定条件下可发生以下变化:
(1)写出反应类型:②___________________,④___________________。
(2)写出反应③的化学方程式:______________________________________;
(3)写出能证明糠醛中含有醛基的一个化学反应方程式_________________________。
若E为高聚物,则其结构简式 ______________________________________。
若E为环状化合物,则其结构简式______________________________________。
(4)糠醛也能与苯酚在一定条件下发生反应生成高分子化合物,原理与甲醛苯酚反应原理相同,试写出糠醛与苯酚的化学反应方程式。