磁性材料氮化铁镍合金可用Fe(NO3)3、Ni(NO3)2、丁二酮肟、氨气、氮气、氢氧化钠、盐酸等物质在一定条件下反应制得。
(1)基态Ni原子的价电子排布式是 。
(2)丁二酮肟(结构式如图所示)中碳原子的杂化方式为 。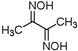
(3)NH3的沸点高于PH3,其主要原因是 。
(4)与N 3- 离子具有相同电子数的三原子分子的空间构型是 。
(5)向Ni(NO3)2溶液中滴加氨水,刚开始时生成绿色Ni(OH)2沉淀,当氨水过量时,沉淀会溶解,生成[Ni(NH3)6]2+的蓝色溶液,则1 mol [Ni(NH3)6]2+含有的σ键为 mol。
(6)下图是一种镍基合金储氢后的晶胞结构示意图。该合金储氢后,含1 mol La的合金可吸附H2的数目为 。
在盛有500mL 1.4mol/L H2SO4溶液的大烧杯中。用锌、铜作电极,用导线连接形成原电池,当电极锌消耗6.5g时,试完成:
(1)写出电极反应式:负极______________________;正极_______________________。
(2)电极上共析出氢气的质量为克。
写出下列化学用语:
(1)由甲烷制取一氯甲烷的化学方程式:__________________________
(2)写出异丁烷的结构简式。
下表是元素周期表的一部分,其中每个数字序号代表一种短周期元素。
请按要求回答下列问题:
(1) 写出②的元素名称;
(2) 将④、⑤和⑥三种元素相比较,金属性最强的是(填元素符号);
(3) 元素③的最高价氧化物对应的水化物的化学式为;
(4) 元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式。
A、B、C、D分别表示含有10个电子的离子A或分子,请回答:
(1)A是由五个原子核组成的阳离子,其化学式是;
(2)B是由两种元素组成的双原子阴离子,其电子式是;
(3)C是只含极性键的四原子分子,其结构式是;
(4)D是由两种元素组成的三原子分子,其分子式是___________。
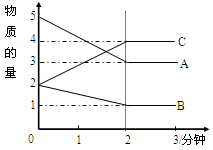
某温度时在密闭容器中A、B、C三种气态物质的物质的量随时间的变化如图所示。则该反应的化学方程式为;2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了_________状态。