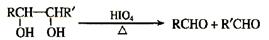根据表中左栏信息,回答右栏有关问题:
| 信 息 |
问 题 |
| ①短周期元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数均不少于最内层电子数。其中X是形成化合物种类最多的元素。 |
(1)X元素的最高价氧化物的电子式是 |
| ②在一定条件下,上述四种元素的单质均能与足量的氧气反应,其中Z元素的氧化物既能溶于稀硫酸,又能溶于浓NaOH溶液。 |
(2)Z元素在元素周期表中位于第_____周期,_____族。 |
| ③Y固体单质与盐酸反应,再向反应后的溶液中加入过量的烧碱溶液,最终溶液中有白色沉淀生成。 |
(3)写出生成白色沉淀的化学方程式 。 |
| ④向上述四种元素的单质的混合物中加入足量的烧碱,固体部分溶解,过滤,向滤液中加入过量的盐酸溶液,最终溶液中有白色沉淀。 |
(4)最终生成白色沉淀的离子方程式为 。 |
| ⑤X、Y、Z、W四种元素的原子半径由大到小的顺序为____________(用元素符号表示) |
下图中 A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物。
根据下图回答问题: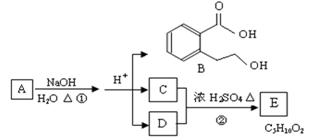
(1)C分子中的官能团名称是: ______________;下列反应中,化合物B不能发生的反应是(填字母序号):
a 加成反应 b取代反应 c消去反应 d酯化反应 e水解反应 f加聚反应。
(2)反应②的化学方程式是 ________。
(3)A的结构简式是 __________________。
(4)同时符合下列三个条件的B的同分异构体的数目有个。
Ⅰ.含有间二取代苯环结构Ⅱ.属于非芳香酸酯Ⅲ.与 FeCl3溶液发生显色反应。
写出其中任意一个同分异构体的结构简式
(5)常温下,将C溶液和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液pH如下表:
| 实验编号 |
C物质的量浓度(mol·L-1) |
NaOH物质的量浓度(mol·L-1) |
混合溶液的pH |
| m |
0.1 |
0.1 |
pH=9 |
| n |
0.2 |
0.1 |
pH<7 |
从m组情况分析,用离子方程式表示该溶液pH=9的原因。
n组混合溶液中离子浓度由大到小的顺序是。
(13分) A~L均为化学实验室中常见的物质,它们有以下转化关系。其中:I是一种黄绿色有毒气体,B、D、E、G均为家庭中常见的物质,常温下,B为无色液体,L是一种具有水果香味的液体。试回答下列问题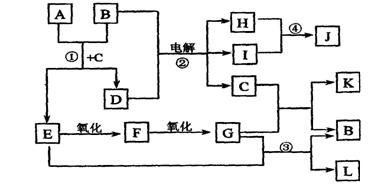
(1)A的名称: C的电子式:
(2)写出反应①的化学反应方程式
写出反应②的离子方程式
(3)实验室以E为原料制取一种植物生长调节剂的化学方程式为: .
A、B、C、D、E五种短周期元素,原子序数依次增大。A元素的单质是自然界最轻的气体,E单质须保存在煤油中。A与B、C分别构成电子数相等的化合物M、N,且M是一种能产生温室效应的最简单的有机气体物质;D元素最外层电子数是次外层电子数的3倍;回答下列问题:
(1)N的电子式为;M分子中含有(填“极性”或“非极性”)键
(2)D与E以1:1形成的化合物与水反应的化学反应方程式
(3)A、B、C、D可形成阳离子和阴离子个数比是1∶1的离子化合物X;A、D、E可形成化合物Y;X与Y以物质的量之比1∶2加热反应,写出反应的化学方程式
反应后水溶液显(填“酸”“碱”或“中”)性,原因是(用离子方程式表示)
(4)由N与D的单质、KOH溶液构成原电池,负极会产生C的单质。则其负极反应为;一段时间后,溶液pH(填“增大”“减小”或“不变”)。 (5)在一定温度下,将4 mol C单质和12 mol A单质通入到体积为2L的密闭容器中,发生反应,2 min达到平衡状态时,A单质的转化率是50%,则用A单质表示该反应的平均速率为;该温度下的平衡常数为K=。
(5)在一定温度下,将4 mol C单质和12 mol A单质通入到体积为2L的密闭容器中,发生反应,2 min达到平衡状态时,A单质的转化率是50%,则用A单质表示该反应的平均速率为;该温度下的平衡常数为K=。
从化学平衡移动的角度分析,提高A单质的转化率可以采取的措施是(选填序号字母)。
a、及时分离出生成物b、平衡后再加入6molA物质c、增大压强d、使用催化剂 e、平衡后再加入2molC物质
分子式为C12H14O2的F有机物广泛用于香精的调香剂。为了合成该物质,某实验室的科技人员设计了下列合成路线: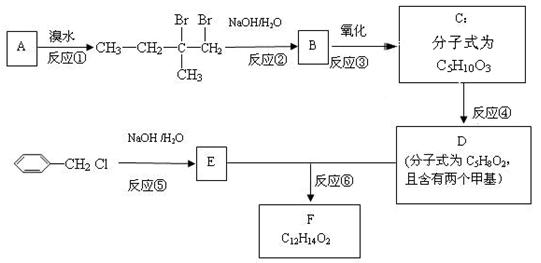
试回答下列问题:
(1)A物质在核磁共振氢谱中能呈现种峰;峰面积比为
(2)C物质的官能团名称
(3)上述合成路线中属于取代反应的是(填编号);
(4)写出反应④、⑤、⑥的化学方程式:④⑤⑥
(5)F有多种同分异构体,请写出符合下列条件的所有结构简式:①属于芳香族化合物,且含有与F相同的官能团;②苯环上有两个取代基,且苯环上的一氯代物只有两种;③其中一个取代基为-CH2COOCH3;
奶油中含有有一种可作香料的化合物A,A中只含C、H、O三种元素。通过红外光谱图分析可知A中含有碳氧双键;通过李比希法分析得到A分子中C、H、O原子个数比为2:4:1,通过质谱仪分析其相对分子质量为88。
已知: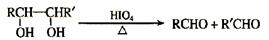
与A相关的反应如下: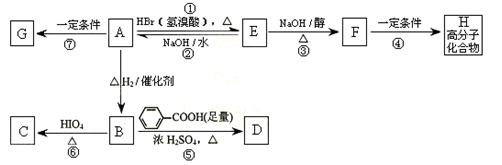
⑴ A的分子式为,H的结构简式为。
⑵上述7步反应中属于取代反应的是(填序号)。
⑶写出B → D反应的化学方程式:。
⑷ B的核磁共振氢谱图中共有个峰。
⑸在空气中长时间搅拌奶油,A可转化为相对分子质量为86的化合物G。G有多种同分异构体,其中符合下列两个条件的同分异构体共有种。
A.无环状结构 B.不含碳碳双键和碳碳叁键
⑹请设计合理方案从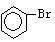 合成OHC(CH2)4CHO(用反应流程图表示,注明反应物、反应条件;无机试剂可自选)。
合成OHC(CH2)4CHO(用反应流程图表示,注明反应物、反应条件;无机试剂可自选)。
反应流程图示例(由乙醇合成聚乙烯):