【2015北京理综化学】氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:

(1)反应Ⅰ的化学方程式是 。
(2)反应Ⅰ得到的产物用I2进行分离。该产物的溶液在过量I2的存在下会分成两层——含低浓度I2的H2SO4层和高浓度的I2的HI层。
①根据上述事实,下列说法正确的是 (选填序号)。
a.两层溶液的密度存在差异
b.加I2前,H2SO4溶液和HI溶液不互溶
c.I2在HI溶液中比在H2SO4溶液中易溶
②辨别两层溶液的方法是 。
③经检测,H2SO4层中c(H+):c(SO42-)=2.06:1。其比值大于2的原因是 。
(3)反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g)△H=+550kJ/mol
它由两步反应组成:i.H2SO4(l)=SO3(g)+H2O(g)△H=+177kJ/mol
ii.SO3(g)分解。
L(L1、L2),X可分别代表压强或温度。下图表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系。

①X代表的物理量是 。
②判断L1、L2的大小关系,并简述理由: 。
( 1 ) 在实验室鉴定氯酸钾晶体和1-氯丙烷中的氯元素,现设计了下列实验操作程序:①滴加AgNO3溶液;②加入NaOH溶液;③加热;④加催化剂MnO2;⑤加蒸馏水过滤后取滤液;⑥过滤后取残渣;⑦用HNO3酸化。
鉴定氯酸钾中氯元素的操作步骤依次是_______________(填序号)
鉴定1-氯丙烷中氯元素的操作步骤依次是_____________(填序号)
( 2 ) 通常用燃烧的方法测定有机物的的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的的质量确定有机物的组成。下图所示的是用燃烧法确定有机物分子式的常用装置。
现准确称取1.8g样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重1.76g,
B 管增重0.36g。请回答:
(1)该有机物的的最简式为__________________;
(2)产生的气体由左向右流向,所选用的各导管口连接的顺序是____________;
(3)E中应盛装什么试剂:_______________;
(4)如果把CuO网去掉,A管重量将_____________;(填“增大”、“减小”、或“不变”)
(5)A、B管内均盛有有固态试剂,B管的作用是______________________;
(6)要确定该有机物的分子式,还必须知道的数据是___________;
A. 消耗液体E的质量 B.样品的摩尔质量 C. CuO固体减少的质量
D. C装置增加的质量 E.燃烧消耗O2的物质的量
(7)在整个实验开始之前,需先让D产生的气体通过整套装置一段时间,其目的是
__________________________________________________。
阅读下列实验内容,根据题目要求回答问题。
某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100mL稀H2SO4溶液;以0.14mol·L-1的NaOH溶液滴定上述稀H2SO4 25.00mL,滴定终止时消耗NaOH溶液15.00mL。
(1)该学生用标准0.14mol·L-1 NaOH溶液滴定硫酸的实验操作如下:
| A.用酸式滴定管取稀H2SO425.00mL,注入锥形瓶中,加入指示剂。 |
| B.用待测定的溶液润洗酸式滴定管 |
| C.用蒸馏水洗干净滴定管 |
| D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2—3cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下 |
E、检查滴定管是否漏水
F、另取锥形瓶,再重复操作一次
G、把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
①滴定操作的正确顺序是(用序号填写);
②该滴定操作中应选用的指示剂是;
③在G操作中如何确定终点?。
(2)碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果(填“偏小”、“偏大”或“恰好合适”)
(3)配制准确浓度的稀H2SO4溶液,必须使用的主要容器是
(4)如有1mol/L和0.1mol/L的NaOH溶液,应用_____ _的NaOH溶液,原因是______________________。
(5)用标准NaOH溶液滴定时,应将标准NaOH溶液注入__(选填“甲”或“乙”)中。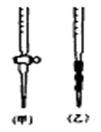
(6)观察碱式滴定管读数时,若滴定前仰视,滴定后俯视,则结果会导致测得的稀H2SO4溶液浓度测定值(选填“偏大”“偏小”或“无影响”)
(7)计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度(计算结果到小数点后二位)。
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组拟用KMnO4溶液滴定的方法,测定该补血剂中铁元素的含量,进行了如下实验:
[查阅资料]
在酸性条件下,用KMnO4标准溶液进行氧化还原滴定,可以测定Fe2+的含量。反应的离子方程式是:Fe2++MnO4-+H+—— Fe3++Mn2++H2O(未配平)
[准备实验用品]
①仪器:a.电子天平,b.滴定管,c.100mL量筒,d.烧杯,e.漏斗,f.250mL容量瓶,g.锥形瓶,h.玻璃棒,i.药匙,j.烧瓶,k.铁架台(带滴定管夹),l.胶头滴管。
②试剂:a.硫酸亚铁补血剂药片,b.高锰酸钾晶体,c.酚酞溶液,d.KSCN溶液,
e.稀硫酸,f.稀盐酸,g.蒸馏水。
[实验步骤]
①称取0.474 g KMnO4晶体,配成250.00 mL水溶液;
②取5片除去糖衣(非还原糖)后的硫酸亚铁补血剂药片(1.500 g),研细后加稀硫酸溶解,配成100.00 mL水溶液。
③用酸式滴定管取待测“补血剂”溶液20.00mL于某容器中。
④盛装标准KMnO4溶液,静置后,读取数据,记录为KMnO4标准溶液体积的初读数。
⑤滴定,并记录KMnO4标准溶液的终读数。再重复滴定2次。
[实验记录]
| 滴定次数 实验数据 |
1 |
2 |
3 |
| V(样品)/mL |
20.00 |
20.00 |
20.00 |
| V(KMnO4)/mL(初读数) |
0.00 |
0.20 |
0.00 |
| V(KMnO4)/mL(终读数) |
15.85 |
15.22 |
14.98 |
[交流与讨论]
(1)准备的实验用品中,不需要的仪器有(填序号);不需要的试剂有(填序号)。
(2)本实验所用的KMnO4标准溶液的物质的量浓度为。
(3)课外小组里有位同学设计了下列四种滴定方式(夹持部分略去),引起了同学们的讨论,最后取得共识,认为最合理的是(填字母序号)。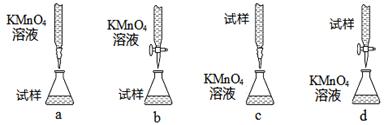
(4)判断滴定终点的依据是。
(5)根据实验数据,计算该补血剂中铁元素的含量。
苯甲酸乙酯(C9H10O2)稍有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等。其制备方法为:
实验步骤如下:
①在100 mL圆底烧瓶中加入12.20 g苯甲酸、25mL乙醇(过量)、20mL环己烷,以及4mL浓硫酸,混合均匀并加入沸石,按左上图所示装好仪器,控制温度在65~70℃加热回流2h。反应时环己烷-乙醇-水会形成“共沸物”(沸点62.6℃)蒸馏出来。再利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞。继续加热,至分水器中收集到的液体不再明显增加,停止加热。
③将烧瓶内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性。
④用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并有机层。加入氯化钙,对粗产品进行蒸馏(装置如图所示)。低温蒸出乙醚后,继续升温,接收210~213℃的馏分。
⑤检验合格,测得产品体积为12.86mL.
回答下列问题:
⑴步骤①中使用分水器不断分离除去水的目的是。
⑵步骤②中应控制馏分的温度在。
| A.65~70℃ | B.78~80℃ | C.85~90℃ | D.215~220℃ |
⑶若Na2CO3加入不足,在步骤④蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是。
⑷蒸馏装置图中仪器A的名称是,在步骤④中加入氯化钙的作用是。
⑸该实验产品的产率为。
实验室可用NH4HCO3和NaCl为原料制备纯碱。请根据下表数据和实验步骤,回答下列问题: 30℃时几种盐的溶解度/g
| NaCl |
NH4HCO3 |
NaHCO3 |
NH4Cl |
Na2SO4 |
(NH4)2SO4 |
CaCl2 |
MgCl2 |
CaSO4 |
| 36.3 |
27.0 |
11.1 |
41.4 |
40.8 |
78 |
51.7 |
26.2 |
0.165 |
制备纯碱的步骤如下:
①配制50 mL约25%的粗食盐水溶液(密度近似为1 g/mL)。
②精制食盐水(粗食盐中含有少量Ca2+、Mg2+、SO42-等杂质),用盐酸将滤液的pH值调至7。
③加热食盐水,将溶液温度控制在30 ─ 35℃。
④在不断搅拌下,分次将研细的NH4HCO3加入食盐水中,加完料后,继续保温、搅拌半小时。
⑤静置,趁热过滤,回收母液。晶体用蒸馏水洗涤两次。
⑥将晶体灼烧,得到纯碱。
(1)步骤①中,配制溶液的最后一步操作是;
(2)步骤②中,SO42-是否需要加入某种试剂除去?,理由是
(3)步骤④中所有操作的共同目的是;
(4)步骤⑤中晶体的洗涤液中主要含有的杂质阳离子是,在通常情况下,检验这种阳离子的实验操作为。