我们学习过常见气体的实验室制法,知道了制取气体的一般思路和方法。
(1)实验室制取气体时,确定发生装置需要考虑的两个因素有 (填序号);
| A.反应物的状态 | B.气体的密度 |
| C.反应的条件 | D.气体的溶解性 |
(2)某实验室的仪器柜里有如下仪器:

写出图中标号①仪器的名称 。实验室用大理石和稀盐酸制备并收集一瓶干燥的二氧化碳时,不可能选择的仪器是 (填序号);
(3)老师问:“如果实验室在没有大理石的情况下能否用碳酸钠粉末与稀盐酸来制取二氧化碳呢?”,大多数同学认为可以,反应的化学方程式为 。为了完成该实验,有四位同学组装了以下发生装置,你认为最合适的一套装置是 (填序号),该装置的最大优点是 。

(4)某实验小组还利用下图装置对实验室制取 的速率快慢进行了研究。他们实验时所用的试剂和使用的反应条件如下表所示:
的速率快慢进行了研究。他们实验时所用的试剂和使用的反应条件如下表所示:
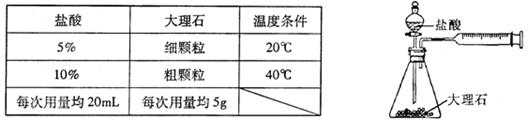
实验小组同学设计的实验方案部分如下表,请根据表中信息帮助填写完整。

实验探究时,他们每次收集 气体均为40mL,则实验中他们还应记录的实验数据是 。
气体均为40mL,则实验中他们还应记录的实验数据是 。
下图是根据某次实验数据作出的 和时间变化的关系曲线,请分析在80秒以后,产生
和时间变化的关系曲线,请分析在80秒以后,产生 逐渐减慢的可能原因: 。
逐渐减慢的可能原因: 。
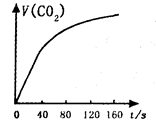
实验室制取少量溴乙烷的装置如右图所示。根据题意完成下列填空:
(1)圆底烧瓶中加入的反应物是溴化钠、乙醇 和1:1的硫酸。配制体积比1:1的硫酸所用的仪器为
和1:1的硫酸。配制体积比1:1的硫酸所用的仪器为
(选填编号)。
a.天平 b.量筒 c.容量瓶 d.烧杯
(2)写出加热时烧瓶中发生的主要反应的两个化学方程式、。
(3)将 生成物导入盛有冰水混合物的试管A中,冰水混合物的作用是。
生成物导入盛有冰水混合物的试管A中,冰水混合物的作用是。
(4)用浓硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质的最佳方法是 (选填编号)。
(选填编号)。
a.蒸馏 b.氢 氧化钠溶液洗涤 c.用四氯化碳萃取 d.用亚硫酸钠溶液洗涤
氧化钠溶液洗涤 c.用四氯化碳萃取 d.用亚硫酸钠溶液洗涤
(5)实验员老师建议把上述装置中的仪器连接部分由橡胶管改成标准玻璃接口,其原因是。
(14分)如图是某研究性学习小组设计制取氯气并以氯气为反应物进行特定反应的装置。
(1)要将C装置接入B和D之间,正确的接法是:a→ → →d。
(2)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处的酒精灯。Cl2通过C装置后进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为______________________。
为了使C装置发挥更好的作用,可向烧杯中加入浓硫酸,加入浓硫酸的作用是_____________________________________________。
(3)D处反应完毕后,关闭旋塞K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是 ,B的作用是______________________。
(4)用量筒量取20 mL E中溶液,倒入已检查完的分液漏斗中,然后再注入10 mL CCl4,盖好玻璃塞(如图),振荡,静置于铁架台上,等分层后取上层液和下层液,呈黄绿色的是 (填“上层液”或“下层液”),再装入如图所示的烧杯中,能使有色布条褪色的是 (填“上层液”或“下层液”)。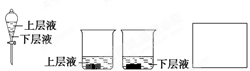
(5)在A、B、C、D、E装置中有一处需要改进,说明需要改进的理由______________________________,并在方框中画出改进后的装置图。
某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
请根据上面流程,回答以下问题:
(1)操作I所用到的玻璃仪器除烧杯.玻璃棒.量筒外,还必须有____________ (填仪器名称),操作II必须用到的仪器是____________(填编号)。
| A.50mL烧杯 | B.50mL量筒 |
| C.25mL碱式滴定管 | D.25mL酸式滴定管 |
(2)洗涤是洗去附着在沉淀上的____________。(写离子符号)
(3)检验沉淀是否已经洗涤干净的操作是________________________。
(4)将沉淀物加热,并置于干燥器中冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是_________。
(5)若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是__________。
(6)有同学认为:上述流程中若不加入氯水,其它步骤不变,仍可达到目的。他的理由是____________。(用化学方程式表示)
某化学兴趣小组为探究铜与浓硫酸的反应,用下图所示装置进行有关实验。
(1)装置D中试管口放置的棉花中应浸一种液体,这种液体是,其作用是。
(2)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是。B中应放置的液体是(填字母)。
a.水 b.酸性KMnO4c.浓溴水 d.饱和NaHSO3
(3)取6.4g铜片和12mL 18.4mol·L-1浓硫酸放在圆底烧瓶中共热, 直到反应完毕,最后发现烧瓶中还有铜片剩余。某同学根据所学的化学知识认为还有一定量的硫酸剩余。
直到反应完毕,最后发现烧瓶中还有铜片剩余。某同学根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是
②下列药品能用来证明反应结束后烧瓶中确实有余酸的是(填字母)。
a.铁粉 b.银粉 c.碳酸氢钠溶液 d.氯化钡溶液
(4)为定量测定余酸物质的量浓度,某同学进行了如下设计:先测定铜片和浓硫酸反应产生的SO2的量,再计算余酸的物质的量浓度。测定SO2的量的方案很多,下列方案可行的是
(填字母)
a.将装置中产生的气体缓缓通过预先称量过盛有碱石灰的干燥管,结束反应后再次称量
b.将装置中产生的气体缓缓通入足量氢氧化钡溶液中,反应完全后过滤、洗涤、干燥、称量沉淀
c.将装置中产生的气体缓缓通入足量硝酸酸化的硝酸钡溶液中,反应完全后过滤,洗涤干燥、称量沉淀
用下列几个实验,可快速制取实验室所需的少量气体,并进 行相关性质实验。(实验装置如右图所示)
行相关性质实验。(实验装置如右图所示)
(1)若A中为30%的H2O2溶液,B中固体为MnO2,C中盛有FeCl2和KSCN的混合液,旋开E后,发现C中溶液变为红色,写出C中发生氧化还原反应的离子方程式。
(2)若A中装有浓盐酸,B中装有固体KMnO4,C中盛有KI淀粉溶液,旋开E后,B中出现黄绿色气体,已知1mol KMnO4发生反应时转移5mol电子。则B中发生反应的化学方程式,C中的现象是。
(3)若B中是生石灰,将A中液体逐滴加入B内,C中盛有铝盐溶液,实验中观察到C溶液中出现白色沉淀,最终沉淀也未溶解。C中发生反应的离子方程式为。