(8分)氨的合成是最重要的化工生产之一。
(1)工业上可用甲烷与水反应得到合成氨用的H2:其热化学反应方程式为CH4(g)+H2O(g)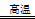 CO(g)+3H2(g) △H4,已知有关反应的能量变化如下图所示:
CO(g)+3H2(g) △H4,已知有关反应的能量变化如下图所示: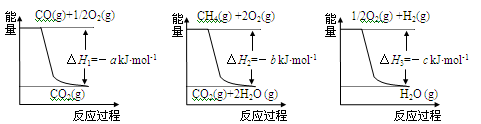
则△H4=______________(用a、b、c表示)
(2)在2个恒压的密闭容器中,同温度下、使用相同催化剂分别进行反应:3H2(g)+N2(g) 2NH3(g),按不同方式投入反应物,保持恒温,反应达到平衡时有关数据为:
2NH3(g),按不同方式投入反应物,保持恒温,反应达到平衡时有关数据为:
| 容 器 |
甲 |
乙 |
| 反应物投入量 |
3 mol H2、2 mol N2 |
6 mol H2、4mol N2 |
| 达到平衡的时间(min) |
t |
5 |
| 平衡时N2的浓度(mol·L-1) |
3 |
c |
①甲容器达到平衡所需要的时间t 5min(填“>”、“<” 或“=”,下同);乙容器达到平衡时N2的浓度c 3 mol·L-1。
②下图中虚线为该反应在使用催化剂条件下,关于起始N2与H2投料比和 H2平衡转化率的关系图。当其他条件完全相同时,用实线画出不使用催化剂情况下H2平衡转化率的示意图。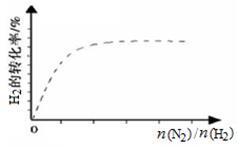
反应3Fe(S)+4H 2O====Fe3O4(s)+4H2(g),在
2O====Fe3O4(s)+4H2(g),在 一可变的容积的密闭容器中进行,试回答:
一可变的容积的密闭容器中进行,试回答:
①增加Fe的量,其正反应速率的变化是(填增大、不变、减 小,以下相同)
小,以下相同)
②将容器的体积缩小一半,其正反应速率,逆反应速率 。
。
③保持体积不变,充入N2使体系压强增大,其正反应速率,逆反应速率。
④保持压强不变,充入N2使容器的体积增大,其正反应速率,逆反应速率。
有两个起始体积相同的密闭容器A和B, A容器有一个可移动的活塞,能使容器内保持恒压;B容器为固定体积。起始时这两个容器分别充入等量的体积比
A容器有一个可移动的活塞,能使容器内保持恒压;B容器为固定体积。起始时这两个容器分别充入等量的体积比
为2 ∶1的SO2和O2的混合气,并使A、B容器中气体体积相等,并保持在
∶1的SO2和O2的混合气,并使A、B容器中气体体积相等,并保持在
400℃条件下发生反应2SO2+O2 2SO3,并达到平衡。
2SO3,并达到平衡。
⑴ 达到平衡所需时间,A容器比B容器_______,两容器中SO2的转化率A比B______。
⑵ 达 到⑴所述平衡后,若向两容器中分别通入数量不多的等量Ar气体,A容器的化学平衡向________移动,B容器的化学平衡________移动
到⑴所述平衡后,若向两容器中分别通入数量不多的等量Ar气体,A容器的化学平衡向________移动,B容器的化学平衡________移动 。
。
⑶ 达到⑴所述平衡后,若向容器中通入等量的原混合气体,重新达到平衡后,A容器中SO3的体积分数________,B容器中SO3的体积分数__________(填变大、变小、不变)。
22.反应A(g)+B(g)  C(g) +D(g)过程中的能量变化如图所示,回答下列问题:
C(g) +D(g)过程中的能量变化如图所示,回答下列问题: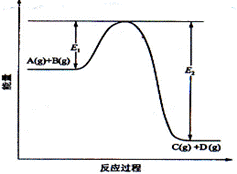
(1)该反应的反应物总能量________生成物的总能量(选填“ 小于”“大于”或“相等”)。
小于”“大于”或“相等”)。
(2)当反应达到平衡时,若升高温度,A的转化率_____(选填“增大”“减小”“不变”原因是____________
____________;若增大压强,则V正 V逆(选填“<”“>”“=”)。
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1____,E2_____(填“增大”“减小”“不变”)。
红磷P(S)和Cl2发生反应生成PCl3和PCl5,反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)
根据上图回答下列问题
(1)P和Cl2反应生成PCl3的热化学方程式:
;
(2)PCl5分解生成PCl3和Cl2的热化学方程:
;温度T1时,在密闭容器中加入0.8mol PCl5 ,反应达到平衡时还剩余0.6mol PCl5 ,其分解率α1等于
(3)P和Cl2分两步反应生成1mol PCl5的△H3=;
P和Cl 2一步反应生成1mol PCl5的△H4△H3(填“大于”,“小于”或“等于”) 。
2一步反应生成1mol PCl5的△H4△H3(填“大于”,“小于”或“等于”) 。
实验题:(本题共9分)某烧碱样品含有少量不与酸作用的杂质,为了滴定其纯度,进行以下滴定操作:
| A.在250 mL的容量瓶中配制250 mL烧碱溶液; | B.用碱式滴定管量取25.00 mL烧碱溶液于锥形瓶中并滴加几滴酚酞做指示剂; | C.在天平上准确称取烧碱样品W g,在烧杯中用蒸馏水溶解; | D.将物质的量浓度为cmol/L的标准盐酸溶液装入酸式滴定管。调整液面记下开始读数为V1 mL;E.在锥形瓶下垫一张白纸,滴定最后一滴至红色刚好消失 为止,半分钟后不恢复红色,记下读数V2 mL。 为止,半分钟后不恢复红色,记下读数V2 mL。 |
就此实验完成下列填空:
(1)正确操作步骤的顺序是:(用编号字母填写)。
( 2)观察滴定管里液面的高度时应注意:。
2)观察滴定管里液面的高度时应注意:。
(3)E步骤的操作中在锥形瓶下垫一张白纸的作用是。
(4)D步骤的操作中液面应调节到,尖嘴部分应。
(5)某学生实验时把锥形瓶用烧碱样品洗涤,使测定的浓度偏高还是偏低?
(6)该烧碱样品纯度的计算式为: