已知A元素原子的L层比B元素原子的L层少3个电子,B元素原子核外电子数比A元素原子核外电子总数多5个,则A、B两元素形成的化合物可表示为
A.BA2 B.BA3 C.A3B2 D.B3A2
已知甲苯的一氯代物有4种,则甲苯与氢气完全加成后产物的一氯代物的种类数是
| A.2种 | B.4种 | C.5种 | D.7种 |
化学在生产和日常生活中有着重要的应用。下列说法正确是
| A.汽车的排气管上装有“催化转化器”,使有毒的CO和NO反应生成N2和CO2 |
| B.向煤中加入适量石灰石,使煤燃烧产生的SO2最终生成CaSO3,可减少对大气的污染 |
| C.高纯度的硅单质广泛用于制作光导纤维 |
| D.大量燃烧化石燃料排放的废气中含CO2、SO2,从而使雨水的pH=5.6形成酸雨 |
【化学一物质结构与性质】
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
试回答下列问题:
(1)请写出元素n的基态原子的价电子排布式,元素O在周期表的位置是,属于区。
(2)k在空气中燃烧产物的分子构型为,中心原子的杂化方式为,该分子是(填“极性”或“非极性”)分子。
(3)第三周期8种元素按单质熔点高低的顺序如左下图,其中序号“8”代表(填元素符号);其中电负性最大的是(填下图中的序号)。
(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如右下图乙所示。则晶胞中i原子的配位数为。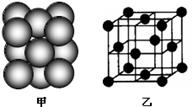
下列离子方程式的书写及评价均合理的是
| 选项 |
离子方程式 |
评价 |
| A |
将2 mol Cl2通入到含1 mol FeI2的溶液中: 2Fe2++2I-+2Cl2===2Fe3++4Cl-+I2 |
正确; Cl2过量,Fe2+、I-均被氧化 |
| B |
用Cu电极电解NaCl溶液阳极的电极反应式: 2Cl--2e-===Cl2↑ |
正确; Cl-优先于OH-放电 |
| C |
过量SO2通入到NaClO溶液中: SO2+H2O+ClO-===HClO+HSO3- |
正确; H2SO3的酸性强于HClO |
| D |
Mg(HCO3)2溶液与足量的NaOH溶液反应: Mg2++2HCO3-+4OH-=== Mg(OH)2 ↓+2CO32-+2 H2O |
正确; Mg(OH)2比MgCO3更难溶 |
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如下图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是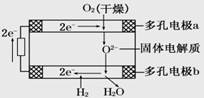
| A.有O2放电的a极为电池的负极 |
| B.O2-移向电池的正极 |
| C.b极对应的电极反应为2H2-4e-+2O2-==2H2O |
| D.a极对应的电极反应为O2+2H2O+4e-==4OH- |