X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为 、 ;
(2)XZ2与YZ2分子的立体结构分别是 和 ,相同条件下两者在水中的溶解度较大的是 (写分子式),理由是_________________;
(3)Q的元素符号是 _____ ,它属于第 _____ 周期,它的核外电子排布式为 _____ ,在形成化合物时它的最高化合价为 _____ ;
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键_________________。
(5)YZ2在固态时为 _____ 晶体,1 mol YZ2中含σ键 _____ mol,π键 _____mol。
537℃、1.01×105Pa 时,往容积可变的密闭容器中充入2mol SO2、 1mol O2,此时容器的体积为200L。向容器中加入催化剂(固体)并保持恒温恒压,发生反应:
2SO2(气)+O2(气) 2SO3(气)
2SO3(气)
达到平衡时,平衡气体中SO3的体积分数为0.91。
试回答下列问题:
(1)工业上二氧化硫的催化氧化采用常压而不采用高压的原因是: _______。
(2)保持上述温度和压强不变,若向容器中只充入2mol SO3并加入固体催化剂。则平衡时,SO2的体积分数是,容器的体积为L。
(3)温度仍保持537℃,容器体积保持200L不变(恒容)。充入a molSO2、b molO2,并加入固体催化剂,反应达平衡时,SO3的体积分数仍为0.91,体系压强为1.01×105Pa。若a:b=2:1,则a=。
在一定条件下,二氧化硫和氧气发生如下反应:
2SO2(g)+ O2 (g)  2SO3(g) ;△H<0
2SO3(g) ;△H<0
(1)写出该反应的化学平衡常数表达式K=
(2)降低温度,该反应K值 ,二氧化硫转化率 ,化学反应速度 (以上均填增大、减小或不变)
下列方法中可以证明2HI(g) H2(g)+I2(g)已达平衡状态的是( )
①单位时间内生成n mol H2的同时生成n mol HI
②一个H-H键断裂的同时有两个H-I键断裂
③百分组成HI%=I2%
④反应速率υ(H2)=υ(I2)=0.5υ(HI)时
⑤ [HI]=[H2]=[I2]=2:1:1
⑥温度和体积一定时,某一生成物浓度不再变化
⑦温度和体积一定时,容器内压强不再变化
⑧条件一定,混合气体的平均相对分子质量不再变化
⑨温度和体积一定时混合气体的颜色不再变化
⑩温度和压强一定时混合气体密度不再变化
在一定温度下,反应2NO2  N2O4达平衡的标志是 。
N2O4达平衡的标志是 。
| A.混合气颜色不随时间的变化 |
| B.数值上v(NO2生成)=2v(N2O4消耗) |
| C.单位时间内反应物减少的分子数等于生成物增加的分子数 |
| D.压强不随时间的变化而变化 |
E.混合气的平均分子量不变
在一容积固定的反应容器中,有一可左右滑动的密封隔板,两侧分别进行如图所示的可逆反应。各物质的起始加入量如下: A、 B和C均为4.0mol, D为 6.5mol, F为2.0mol,设E为xmol,x在一定范围内变化时,均可以通过调节反应器的温度,使两侧反应都达到平衡,并且隔板恰好处于反应器的正中间位置。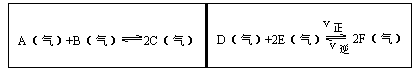
①若x=4.5,则右侧反应在起始时向______方向进行,欲使起始反应维持向该方向进行,则x的取值范围为____ 。
②若x分别为4.5和5.0,则在这两种情况下,当反应达平衡时,A的物质的量是否相等?______,其理由是______。