下图是锌片和铜片在稀硫酸中所组成的原电池装置,c、d为两个电极。下列有关的判断不正确的是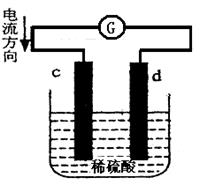
| A.电池工作的过程中,d电极上产生气泡 |
| B.电池工作时,溶液中SO42-向d移动 |
| C.c为负极,发生氧化反应 |
| D.电池工作的过程中,溶液中SO42-浓度基本不变 |
下列叙述中的前后两个量之比为1 :2的是
| A.液面在 “ 0 ” 刻度时,25mL碱式滴定管和50mL碱式滴定管所盛液体的体积 |
| B.相同温度下,0.1mol /L乙酸溶液与0.2mol /L乙酸溶液中,c(H+)之比 |
C.氨水与(NH4)2SO4溶液混合后pH=7的溶液中,c(NH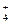 ): c(SO ): c(SO ) ) |
| D.相同温度下,pH=12的Ba(OH)2与pH=12的KOH溶液中,c〔(Ba(OH)2〕: c(KOH) |
已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图所示,下列说法正确的是
| A.Z元素的原子半径可能比Y元素的小 |
| B.W的原子序数可能是Y的原子序数的2倍 |
| C.W的气态氢化物的稳定性一定比Y的强 |
| D.Z的化学活泼性一定比X强 |
“分类”是一种思想方法,在化学发展中起到了重要作用。下列分类标准合理的是
①根据水溶液能否导电将化合物分为电解质和非电解质
②根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
④根据反应中的热效应将化学反应分为放热反应和吸热反应
| A.②④ | B.①② | C.①③ | D.③④ |
把aL含硫酸铵和硝酸铵的混合液分成两等份,一份需用b mol烧碱刚好把氨全部赶出,另一份与氯化钡溶液反应时,消耗c mol氯化钡,由此可知原溶液中N03-的物质的量浓度是(单位:mol·L—1)
A.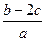 |
B.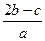 |
C.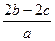 |
D.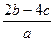 |
将一定量的镁和铝分别与足量的盐酸反应,若放出氢气的质量相等,则参加反应的镁和铝的物质的量之比为
| A. 1:1 | B.2:3 | C.3:2 | D.8:9 |