已知氯酸钾和亚硫酸氢钠发生氧化还原反应时,生成-1价的氯和+6价的硫的化合物,反应速率v和反应时间t的关系如图所示。已知这个反应的反应速率随溶液中氢离子浓度增大而加快,试解释: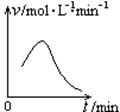
(1)反应开始后,反应速率加快的原因是______________________。
(2)反应后期,反应速率下降的原因是________________________。
(10分)现有A、B两种烃,已知A的分子式为C5Hm,而B的最简式为C5Hn(m、n均为正整数)。
(1)下列关于烃A和烃B的说法中不正确的是 (填字母编号)
a.烃A和烃B可能互为同系物
b.烃A和烃B可能互为同分异构体
c.当m=12时,烃A一定为烷烃
d.当n=11时,烃B可能的分子式有两种
e.烃A和烃B可能都为芳香烃
(2)若烃A为链状烃,且分子中所有碳原子都在一条直线上,则A的结构简式为 。
(3)若烃A为链状烃,分子中所有碳原子不可能都在同一平面上。在一定条件下,1mol A最多只能与1mol H2发生加成反应。写出烃A与氢气完全加成后的产物名称 。
(4)若烃B为苯的同系物,取一定量的烃B完全燃烧后,生成物先通过足量浓硫酸,浓硫酸增重1.26g,再通过足量碱石灰,碱石灰增重4.4g,则烃B的分子式为 。若其苯环上的一溴代物只有一种,则符合条件的烃B有 种。
化合物E是一种化工产品,可以通过下图所示的路线合成:
已知:
(1)化合物II的结构简式为:
(2)写出化合物III与新制氢氧化铜反应的化学方程式: ;反应类型是_________。化合物III与溴水发生反应的方程式是____________________,
(3)下列说法正确的是
| A.化合物I遇氯化铁溶液能显色 |
| B.化合物II能与NaHCO3溶液反应 |
| C.1mol化合物III最多能与3mol H2反应 |
| D.1mol化合物E完全燃烧消耗9.5mol O2 |
(4)有机物R(C9H9ClO3)经过反应也可制得化合物E,R可能的结构简式是__________,则R在NaOH醇溶液中反应的化学方程式为 。
(5)化合物E发生加聚反应产生高聚物F,F的结构简式是_______化合物E发生缩聚反应产生高聚物W,该反应的方程式是______
甲醇是主要的化学工业基础原料和清洁液体燃料。工业上可以用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
| 化学反应及平衡常数 |
温度/℃ |
||
| 500 |
800 |
||
①2H2(g)+CO(g)  CH3OH(g)△H1 CH3OH(g)△H1 |
K1 |
2.5 |
0.15 |
②H2(g)+CO2(g)  CO(g) +H2O(g)△H2 CO(g) +H2O(g)△H2 |
K2 |
1.0 |
2.50 |
③3H2(g)+CO2(g)  CH3OH(g)+H2O(g)△H3 CH3OH(g)+H2O(g)△H3 |
K3 |
||

(1)反应①的反应热△H1 0(填“>”、“<”或“=”);
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如图1所示。则平衡状态由A变到B 时,平衡常数K(A)______K(B) (填“>”、“<”或“=”);
(3)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=___________(用K1、K2表示)。500℃时测得反应③在某时刻H2(g)、CO2(g) 、CH3OH(g)、H2O(g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15,则此时v(正)______v(逆) (填“>”、“<”或“=”);
(4)在3L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是___________;当曲线Ⅰ变为曲线Ⅲ时,改变的条件是__________________;
(5)若以甲醇为原料制成燃料电池,在碱性介质中负极的电极反应式为____ 。正极的电极反应式是_________________。
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素。A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子。
(1)基态的F3+核外电子排布式是 。
(2)B的气态氢化物在水中的溶解度远大于A、C的气态氢化物,原因是 。
(3)化合物FD3是棕色固体、易潮解、100℃左右时升华,它的晶体类型是 ;该晶体的结构式是 ;化合物ECAB中的中的阴离子与AC2互为等电子体,该阴离子的电子式是 。

(4)FD3与ECAB溶液混合,得到含多种配合物的血红色溶液,其中配位数为5的配合物的化学式是 。
(5)化合物EF[F(AB)6]是一种蓝色晶体,右图表示其晶胞的 (E+未画出)。该蓝色晶体的一个晶胞中E+的个数为 。
(E+未画出)。该蓝色晶体的一个晶胞中E+的个数为 。
(6)B元素的具有18个电子的氢化物可用作火箭燃料,其原理是:B2O4(l)+2B2H4(l)=3B2(g)+4H2O(g),若反应中有1mol B的氢化物发生反应,则形成的π键有 mol。配合物Y的结构如图所示,Y中含
有 (填序号);
A.极性共价键B.非极性共价键
C.配位键D.氢键
Y中碳原子的杂化方式有 。
(15分)A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解。各种物质之间的转化关系如图所示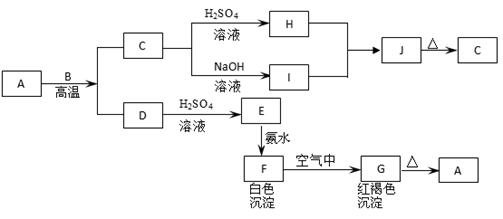
(1)(每空1分,共4分)写出下列物质的化学式:
A________,E____________,I____________,G____________.
(2)(每空2分,共10分)按要求填空:
①A与B在高温条件下生成C和D的化学方程式______________.
②H与I转化为J离子方程式______________.
③F在空气中转化为G的化学方程式___________________________;
④在工业上制取B的化学方程式是:______________________;
⑤若冶炼金属B所需要的电能由甲醇燃料电池提供,反应过程中的能量损耗不计,则产生4mol的D,消耗的燃料的质量是______________。