稀土是一种不可再生的战略性资源,被广泛应用于电子信息、国防军工等多个领域。一种从废弃阴极射线管(CRT)荧光粉中提取稀土元素钇(Y)的工艺流程如下:
已知:①废弃CRT荧光粉的化学组成(某些不参与反应的杂质未列出)如下表所示;
②不同离子沉淀的pH如图所示。
(1)步骤I中进行原料预处理的目的为_____________。
(2)步骤Ⅱ中有黄绿色气体产生,该反应的化学方程式为_______________。
(3)步骤Ⅲ中发生的主要反应的离子方程式为_______________。
(4)步骤Ⅳ中除杂试剂DDTC除去的杂质离子有______,其不能通过直接加碱的方法除去,原因为_____。
(5)步骤V中Y3+沉淀完全时,需保证滴加草酸后的溶液中c(C2O42-)不低于_______mol/L。
(已知:当离子浓度小于10-5mol/L时,沉淀就达完全;Ksp[Y2(C2O4)3]=8.0×10-28)
(6)步骤Ⅵ中草酸钇隔绝空气加热可以得到Y2O3,该反应的化学方程式为___________。
(12分)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是。
(2)烧杯间填满碎纸条的作用是。
(3)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等、不相等”),所求中和热(填“相等、不相等”),简述理由。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会;(填“偏大”、“偏小”、“无影响”)。
(14分) 孔雀石呈绿色,是一种名贵的宝石。其主要成分是xCu(OH)2·yCuCO3。某兴趣小组为探究孔雀石组成,利用下图所示的装置(夹持仪器省略)进行实验: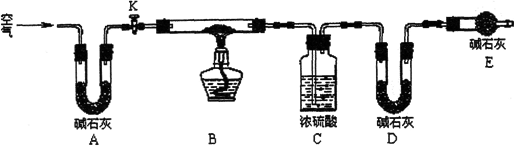
步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于硬直玻璃管中。
步骤2:称量相关装置的质量,打开活塞K,鼓入空气,一段时间后关闭。
步骤3:加热装置B直至装置C中无气泡产生。
步骤4:_________________________ (请补充该步操作内容)。
步骤5:冷却至室温,称量相关装置的质量。
(1)孔雀石热分解的化学方程式_____________________________。
(2)装置A的作用是__________________;若无装置E,则实验测定的x/y的值将__________(选填“偏大”、“偏小”或“无影响”)。
(3)某同学在实验过程中采集了如下数据:
| A.反应前玻璃管与样品的质量163.8g |
| B.反应后玻璃管中残留固体质量20g |
| C.装置C实验后增重2.25g |
| D.装置D实验后增重5.5g |
为测定x/y的值,你认为可以选用上述所采集数据中的_________________
(写出所有组合的字母代号)任一组即可进行计算,并根据你的计算结果,写出孔雀石组成的化学式________。
(16分)某学习小组拟以下列合成路线合成1﹣丁醇:
CH3CH=CH2+CO+H2 CH3CH2CH2CHO
CH3CH2CH2CHO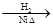 CH3CH2CH2CH2OH
CH3CH2CH2CH2OH
已知:①HCOOH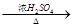 CO↑+H2O(HCOOH还原性强) ②RCH=CH2
CO↑+H2O(HCOOH还原性强) ②RCH=CH2 RCOOH+CO2+H2O
RCOOH+CO2+H2O
请填写下列空白: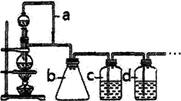
(1)利用如图装置可以制备纯净干燥的CO,则a装置的作用是______________,若无b装置可能产生的后果是________, c装置中发生反应的离子方程式为_______________________________
(2)以2-丙醇为原料可以制备丙烯,化学反应方程式__________________________
在所得丙烯气体中还含有少量SO2、CO2及水蒸气。用以下试剂可以检验四种气体,则混合气体通过试剂的顺序依次是________________(填序号)。
①饱和Na2SO3溶液;②酸性KMnO4溶液;③石灰水:④无水CuSO4;⑤品红溶液
(3)正丁醛经催化加氢得到含少量正丁醛的1﹣丁醇粗品。为提纯1﹣丁醇,该小组设计出如下提纯路线:
已知:①R—CHO+NaHSO3(饱和)→RCH(OH)SO3Na↓:
②沸点:乙醚34℃,1-丁醇:118℃。
则操作1为___________,操作2为_____________,操作3为___________。
甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究。
| 操作 |
现象 |
通入氯气至过量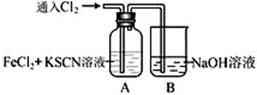 |
I.A中溶液变红 II.稍后,溶液由红色变为黄色 |
(1)B中反应的离子方程式是。
(2)A中溶液变红的原因是。
(3)为了探究现象II的原因,甲同学进行如下实验。
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在。
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。甲同学的实验证明产生现象II的原因是SCN—与Cl2发生了反应。
(4)甲同学猜想SCN—可能被Cl2氧化了,他又进行了如下研究。
资料显示:SCN—的电子式为 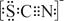 。
。
①甲同学认为SCN—中碳元素没有被氧化,理由是。
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN—中被氧化的元素是。
③通过实验证明了SCN- 中氮元素转化为NO3-,他的实验方案是。
④若SCN—与Cl2反应生成1 mol CO2,则转移电子的物质的量是mol。
下图是丁烷裂解的实验流程:(提示:丁烷在一定条件下裂解的可能方程式为:
C4H10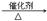 C2H6+C2H4, C4H10
C2H6+C2H4, C4H10 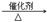 CH4+C3H6)
CH4+C3H6)
连接好装置后,需进行的实验操作有:①给D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等…‥
(1)这三步操作的先后顺序依次是;
(2)简要说明排空气的方法______________。
(3)写出甲烷与氧化铜反应的化学方程式
(4)若对E装置中的混合物(溴水足量),再按以下流程实验:
①分离操作Ⅰ和Ⅱ的名称分别是:Ⅰ______Ⅱ______,Na2SO3溶液的作用是(用离子方程式表示).
②已知B的碳原子数大于A的碳原子数请写出B的结构简式.
(5)假定丁烷完全裂解当(E+F)装置的总质量比反应前增加了0.7 g, G装置的质量减少了1.76 g,则丁烷的裂解产物中甲烷和乙烷的物质的量之比n (CH4) : n (C2H6) =______(假定流经D、G装置中的气体能完全反应)