下列各组元素均属于p区元素的是
| A.H、He、N | B.O、S、P |
| C.Fe、Ar、Cl | D.Na、Li、Mg |
化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如图所示,计算反应4-8 min间的平均反应速率和推测反应16 min时反应物的浓度,结果应是( ) 
| A.2.5 μmol ▪L-1▪min-1和2.0μmol ▪L-1 | B.2.5μmol ▪L-1▪min-1和2.5μmol ▪L-1 |
| C.3.0μmol ▪L-1▪min-1和3.0μmol ▪L-1 | D.5.0μmol ▪L-1▪min-1和3.0μmol ▪L-1 |
某探究小组利用丙酮的溴代反应(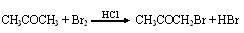 )来研究反应物浓度与反应速率的关系。反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据:
)来研究反应物浓度与反应速率的关系。反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据:
| 实验 序号 |
初始浓度c/mol·l-1 |
溴颜色消失所需时间t/s |
||
| CH3COCH3 |
HCl |
Br2 |
||
| ① |
0.80 |
0.20 |
0.0010 |
290 |
| ② |
1.60 |
0.20 |
0.0010 |
145 |
| ③ |
0.80 |
0.40 |
0.0010 |
145 |
| ④ |
0.80 |
0.20 |
0.0020 |
580 |
分析实验数据所得出的结论不正确的是()
A.增大c(CH3COCH3),υ(Br2)增大 B.实验②和③的υ(Br2)相等
C.增大c(HCl),υ(Br2)增大 D.增大c(Br2),υ(Br2)增大
将一定量的固体Ag2SO4置于容积不变的容器中(装有少量V2O5),在某温度下发生反应:Ag2SO4(s) Ag2O(s)+SO3(g) ,2 SO3(g)
Ag2O(s)+SO3(g) ,2 SO3(g) 2 SO2(g)+O2(g)。反应经过10 min达到平衡,测得c(SO3)=0.4 mol/L、c(SO2)=0.1 mol/L,则下列叙述中不正确的是
2 SO2(g)+O2(g)。反应经过10 min达到平衡,测得c(SO3)=0.4 mol/L、c(SO2)=0.1 mol/L,则下列叙述中不正确的是
| A.容器里气体的密度为40 g/L |
| B.SO3的分解率为20% |
| C.在这10 min内的平均速率为υ(O2)=0.005 mol•L-1•min-1 |
| D.化学反应速率:υ(Ag2SO4)=υ(SO3) |
已知NH3·H2O(aq)与H2SO4(aq)反应生成1mol正盐的反应热△H= -24.2kJ/moL;稀盐酸与稀氢氧化钠溶液反应的中和热△H= -57.3kJ/mol。则NH3•H2O在水溶液中电离的△H等于
| A.-69.4kJ/mol | B.-45.2 kJ/mol | C.+69.4kJ/mol | D.+45.2 kJ/mol |
下列事实不能用勒夏特列原理解释的是()
| A.开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| B.钢铁在潮湿的空气中容易生锈 |
| C.实验室中常用排饱和食盐水的方法收集氯气 |
| D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |