一定温度下在容积恒定的密闭容器中,进行如下可逆反应:
A(s)+2B(g) C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是
C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是
①混合气体的密度不再变化时
②容器内气体的压强不再变化时
③混合气体的总物质的量不再变化时
④B的物质的量浓度不再变化时
⑤混合气体的平均相对分子质量不再改变的状态
⑥当V正(B) = 2V逆(C)
A.①④⑤⑥
B.②③⑥
C.②④⑤⑥
D.只有④
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是
| A.相对于途径①,途径②更好地体现了绿色化学思想 |
| B.Y可以是葡萄糖溶液 |
| C.CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体 |
| D.将CuSO4溶液蒸发浓缩、冷却结晶,可制得胆矾晶体 |
向59.2gFe2O3和FeO的混合物中加入某浓度的稀硝酸1.0L,固体物质完全反应,生成NO和Fe(NO3)3.在所得溶液中加入1.0mol/L的NaOH溶液2.8L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为85.6g.下列有关说法错误的是
| A.Fe2O3与FeO的物质的量之比为1:6 |
| B.硝酸的物质的量浓度为3.0 mol/L |
| C.产生的NO在标准状况下的体积为4.48 L |
| D.Fe2O3,FeO与硝酸反应后剩余HNO3为0.2 mol |
下列说法正确的是
| A.Na2CO3溶液c(Na+)与c(CO32-)之比为2:1 |
| B.pH=2和pH=1的硝酸中c(H+)之比为1:10 |
| C.0.2mol/L与0.1mol/L醋酸中c(H+)之比为2:1 |
| D.pH=1的硫酸中加入等体积0.1mol/L的BaCl2溶液,两者恰好完全反应 |
用压强传感器探究生铁在pH=2和pH=4醋酸溶液中发生腐蚀的装置及得到的图象如下:分析图象,以下结论错误的是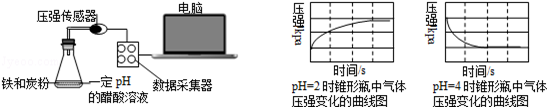
| A.溶液pH≤2时,生铁发生析氢腐蚀 |
| B.在酸性溶液中生铁可能发生吸氧腐蚀 |
| C.析氢腐蚀和吸氧腐蚀的速率一样快 |
| D.两溶液中负极反应均为:Fe﹣2e﹣=Fe2+ |
如图W、X、Y、Z为四种物质,若箭头表示能一步转化的常见反应,其中常温下能实验图示转化关系的是
| 选项 |
W |
X |
Y |
Z |
 |
| A |
S |
SO2 |
SO3 |
H2SO4 |
|
| B |
Na |
Na2O2 |
NaOH |
NaCl |
|
| C |
Al |
AlCl3 |
NaAlO2 |
Al2(SO4)3 |
|
| D |
Fe |
FeCl3 |
Fe(OH)2 |
FeCl2 |