下列关于化学反应速率说法中不正确的是
| A.反应速率用于衡量化学反应进行的快慢 |
| B.决定反应速率的主要因素是反应物的性质 |
| C.可逆反应达到化学平衡状态时,正、逆反应的速率都为0 |
| D.增大反应物的浓度、提高反应温度都能增大反应速率 |
下列有关结构和性质的说法中,正确的是
| A.酸性:HCl>H2S,所以,非金属性:Cl>S |
| B.元素原子的电子层数越多,越容易得电子,非金属性越强 |
| C.同周期主族元素的原子形成的简单离子电子层结构相同 |
| D.同周期第材ⅡA族与第IIIA族的元素原子序数之差不一定为1 |
化学实验中,常将溶液或试剂进行酸化,下列酸化处理的措施中正确的是()
A.定性检验SO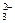 ,可用HNO3酸化的BaCl2溶液 ,可用HNO3酸化的BaCl2溶液 |
| B.为了提高KMnO4溶液的氧化能力,用盐酸将其酸化 |
| C.检验某溶液中是否含Cl – ,用HNO3酸化的AgNO3溶液 |
| D.配制FeCl2溶液时通常加少量H2SO4酸化,减小其水解程度 |
下列各组离子中,在碱性溶液中共存,且加入盐酸过程中,会产生气体和沉淀的是()
| A.Na+、NO3-、AlO2-、SO42- | B.Na+、NO3-、SiO32-、K+ |
| C.K+、Cl-、AlO2-、CO32- | D.K+、Cl-、HCO3-、Ca2+ |
下图装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体,该装置可用于()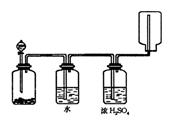
| A.二氧化锰和双氧水反应生成氧气 | B.浓氨水和生石灰混合生成氨气 |
| C.Na2SO3和浓H2SO4混合生成SO2 | D.锌粒与稀盐酸混合生成H2 |
化学与科学、技术、社会、环境密切相关。下列说法中,你认为正确的是()
①加热能杀死甲型 H1N1 流感病毒是因为病毒的蛋白质受热变性
②可用铝制容器存放浓硝酸,是因为常温下浓硝酸与铝不反应
③光缆在信息产业中有广泛应用,制造光缆的主要材料是单质硅
④结构陶瓷碳化硼(B4C3)常用于制造切削工具,它是一种新型无机非金属材料,属于原子晶体
⑤金刚石是自然界中硬度最大的物质,不可能与氧气发生反应
⑥玻璃、水泥的生产都要用石灰石做原料
⑦Na2O2可用于呼吸面具中作为氧气的来源
| A.①⑤⑦ | B.④⑥⑦ | C.②③⑤ | D.③④⑥ |