分枝酸可用于生化研究,其结构简式如图。下列关于分枝酸的叙述正确的是
| A.分子中含有2种官能团 |
| B.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同 |
| C.1mol分枝酸最多可与3molNaOH发生中和反应 |
| D.可与乙醇、乙酸反应,且反应类型相同 |
下列说法正确的是
| A.同温同压下,H2 + Cl2 = 2HCl在光照和点燃条件的△H不同 |
| B.铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| C.天然气、沼气和水煤气分别属于化石能源、可再生能源和一级能源 |
| D.元素原子的核外电子排布呈周期性变化是元素性质呈现周期性变化的根本原因 |
下列化学用语正确的是
A.硫原子的原子结构示意图: |
B.过氧化钠的电子式:Na+[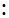 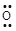 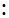 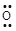 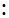 ]2-Na+ ]2-Na+ |
C.原子核内有8个质子、10个中子的氧原子: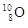 |
| D.HClO的结构式为 H—Cl—O |
2014年是门捷列夫诞辰180周年,下列事实不能用元素周期律解释的只有
| A.相对原子质量:Ar > K | B.碱性:KOH > NaOH |
| C.酸性:HClO4 > H2SO4 | D.元素的金属性:Mg > Al |
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,其负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法正确的是
A.该电池的负极反应为  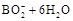 |
| B.电池放电时Na+从b极区移向a极区 |
| C.每消耗3 mol H2O2,转移的电子为3 mol |
| D.电极a采用MnO2作电极材料 |
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g) CO2(g)+H2(g)。反应过程中测定的部分数据见下表(表中
CO2(g)+H2(g)。反应过程中测定的部分数据见下表(表中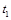 <
<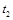 )。下列说法正确的是
)。下列说法正确的是
A.反应在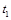 min内的平均速率为 min内的平均速率为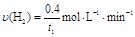 |
| B.温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应 |
C.保持其他条件不变,若向平衡体系中再通入0.20mol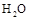 ,与原平衡相比,达到新平衡时CO和 ,与原平衡相比,达到新平衡时CO和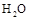 的转化率均增大 的转化率均增大 |
D.保持其他条件不变,若起始时向容器中充入0.60molCO和1.20 mol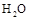 ,则到达平衡时, ,则到达平衡时,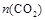 ="0.40" mol ="0.40" mol |