下列叙述中正确的是( )
| A.明矾、硫酸铁都可以用于净水,但净水原理不同 |
| B.粗铝做阳极,硫酸铝溶液做电解液,电解精炼铝 |
| C.工业制硫酸中,将黄铁矿粉碎是为了提高黄铁矿的平衡转化率 |
| D.含有最高价元素的化合物,不一定有强氧化性 |
常温下,下列各组粒子在指定溶液中可能大量共存的是()
| A.氨水中:Al3+、Cl-、I-、SO42- | B.pH=2的溶液中:K+、Cu2+、Cl-、NO3- |
| C.食盐水中:Mg2+、Fe(OH)2、Br-、CO32- | D.无色溶液:NO3-、SO2、NH4+、Na+ |
在高压下氮气会聚合生成高聚氮,这种高聚氮的晶体中每个氮原子都通过三个单键与其它氮原子结合并向空间发展构成立体网状结构(如图)。已知晶体中N — N键的键能为160kJ·mol-1 ,而N ≡ N的键能为942kJ·mol-1 。则下列有关说法正确的是 ( )
| A.高聚氮与氮气互为同位素 |
| B.14g高聚氮含3.01×1023个氮原子 |
| C.高聚氮中氮原子间的化学键为非极性键 |
| D.高聚氮转变成氮气是氧化还原反应 |
常温下,0.1mol/L的氨水pH=11,下列叙述错误的是
| A.向该溶液中加水稀释:c(OH—)/c(NH3·H2O )增大 |
| B.0.lmol/L氨水与0.lmol/LH2SO4溶液等体积混合后所得溶液中:c(NH4+)+c(H+)=2c(SO42—)+c(OH—) |
| C.0.1mol/L氨水与0.05mol/LHCl溶液等体积混合后所得溶液中:c(NH4+)+n(NH3)+n(NH3·H2O)=2n(Cl—) |
| D.浓度均为0.1mol/L氨水和NH4Cl溶液等体积混合后,若溶液呈碱性,则 |
c(NH3·H2O)>c(Cl—)>c(NH+)>c(OH—)>c(H+)
在密闭容器中,可逆反应3X(g)+Y(s) 2Z(g);△H<0,达到平衡后,仅改变横坐标条件,下列图像正确的是
2Z(g);△H<0,达到平衡后,仅改变横坐标条件,下列图像正确的是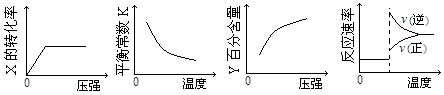
A B C D