【化学——选修化学与技术】明矾石经处理后得到明矾[ KAl(SO4)2·12H2O]。从明矾制备Al、K2SO4和H2SO4的工艺过程如下所示:

焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S=2K2SO4 +2Al2O3+9SO2+48H2O
请回答下列问题:
 (1)在焙烧明矾的反应中,还原剂是 ;
(1)在焙烧明矾的反应中,还原剂是 ;
(2)从水浸后的滤液中得到K2SO4晶体的方法是 ;
(3)A12O3在一定条件下可制得AIN,其晶体结构如图所示,该晶体中Al的配位数是 ;

(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是 ;
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101 kPa时:
2SO2(g) +O2(g) 2SO3(g) △H1= 一197 kJ/mol;
2SO3(g) △H1= 一197 kJ/mol;
2H2O (g)=2H2O(1) △H2=一44 kJ/mol;
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) △H3=一545 kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式是 ;
(6)焙烧948吨明矾(M=474g/mol ),若SO2的利用率为96%,可生产质量分数为98%的硫酸 吨。
将0.1mol有机化合物A与标准状况下5.6L氧气混合,一定条件下两者完全反应,只有CO、CO2和H2O三种产物,将全部产物依次通入足量的浓硫酸和碱石灰中,浓硫酸增重5.4克,碱石灰增重4.4克,还有标准状况下2.24L气体的剩余,求:
(1)有机化合物A的分子式(要求写出推理过程);
(2)若有机化合物A能与钠反应放出氢气,请写出A的结构简式;
(3)写出所有比A多一个—CH2—原子团的同系物的结构简式。
由短周期元素组成的甲、乙和丙均为中学常见物质,一定条件下,存在转化关系: 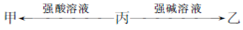
(1)若甲、乙、丙都是单质,甲、乙是同种气体,丙元素的原子结构示意图为;丙单质性质活泼,但由其制成的容器可用于储运浓硫酸,原因是。工业中制取丙的化学方程式:
(2)若甲、乙是同种有机物,体积分数为75%该有机物的水溶液常用于医疗消毒。写出分子中含有4个碳原子的丙转化为甲的化学方程式:
(3)若甲、乙是不同种气体,乙能使湿润的红色石蕊试纸变蓝。
①写出丙→甲反应的离子方程式:(任写一个)
②0.1mol乙与CuO(s)完全反应,得到一种气态单质、一种固态单质和一种液态化合物,放出14.7kJ的热量。该反应的热化学方程式为。
写出下列化学反应方程式:
(1)用电石制备乙炔:。
(2)乙醛与银氨溶液发生银镜反应:。
(3)将灼热的铜丝浸入少量乙醇液体中:。
(4)甲苯与浓硝酸和浓硫酸混合液共热生成三硝基甲苯:。
(5)1,3-二溴-2,3-二甲基丁烷与NaOH的醇溶液共热:。
取未知天然氨基酸A 66.50g进行元素分析,与强碱溶液共热,在标准状况下收集到N25.60L(假设氮全部转化)。已知氨基酸1个分子中含有一个氮原子,又取2.66gA溶于水配成溶液,用0.80mol/LNaOH溶液滴定耗去50.00mL恰好中和。试求:
(1)氨基酸A的摩尔质量
(2)氨基酸A分子中含羧基的个数
(3)求氨基酸A的化学式;请写出A具有对称结构M氨基酸的简式。
某链烃3.6g和Cl2发生取代反应,控制反应条件使其仅生成一氯代物,将反应生成的气体(一氯代物为液体)用NaOH溶液吸收恰好和0.1mol·L-1 NaOH溶液500mL完全反应,试解答下列问题:
(1)求该烃的相对分子质量;
(2)若该烃既不能使酸性KMnO4溶液褪色,又不能使溴水褪色,试求该烃的分子式。
(3)若该烃的一氯代物只有一种,试确定该烃的结构简式 (要求写出计算过程)