下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 |
实验 |
现象 |
结论 |
| A |
将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 |
有气体生成,溶液呈血红色 |
稀硝酸将Fe氧化为Fe3+ |
| B |
将铜粉加入1.0mol·L-1Fe2(SO4)3溶液中 |
溶液变蓝、有黑色固体出现 |
金属铁比铜活泼 |
| C |
用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 |
熔化后的液态铝滴落下来 |
金属铝的熔点较低 |
| D |
将AlCl3溶液逐渐滴入到NaOH溶液中 |
刚开始不产生白色沉淀,而后产生白色沉淀 |
AlO2—与Al3+反应可以生成白色沉淀 |
(届山东省日照市高三3月模拟考试理综化学试卷)
CPAE是蜂胶的主要活性成分,由咖啡酸合成CPAE路线如下: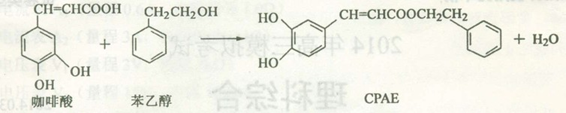
下列说法正确的是
| A.苯乙醇属于芳香醇,它与邻甲基苯酚互为同系物 |
| B.1 molCPAE最多可与含3 mol NaOH的溶液发生反应 |
| C.用FeCl3溶液可以检测上述反应中是否有CPAE生成 |
| D.咖啡酸、苯乙醇及CPAE都能发生取代、加成和消去反应 |
(届浙江省杭州市杭州学军中学高三第二次月考化学试卷)
α,β,γ和δ四种生育三烯酚是构成维生素E的主要物质,下列叙述中不正确的是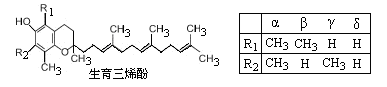
| A.α和δ两种生育三烯酚互为同系物,β和γ两种生育三烯酚互为同分异构体 |
| B.四种生育三烯酚均可使酸性高锰酸钾溶液褪色 |
| C.四种生育三烯酚的结构中均不存在手性碳原子 |
| D.1molα生育三烯酚最多可消耗6molH2 |
(2013-2014学年山东省济宁市嘉祥一中高三3月质检化学试卷)
以下烃中二氯代物只有两种的是()
| A.(CH3)2CHCH3 | B.CH3CH2CH3 | C.CH3CH2CH2CH3 | D.C(CH3)4 |
(2013-2014学年山东省济宁市嘉祥一中高三3月质检化学试卷)
要证明氯乙烷中氯元素的存在可进行如下操作,其中顺序正确的是()
①加入AgNO3溶液;②加入NaOH溶液;③加热;④加入蒸馏水;⑤加入HNO3酸化
| A.②③⑤① | B.④③⑤① | C.④①⑤ | D.②③①⑤ |
(2014届北京市顺义区高三第一次统练考试化学试卷)
下列实验操作不能达到预期目的的是
| 实验目的 |
操作 |
|
| A |
欲比较水和乙醇中羟基氢的活泼性 |
用金属钠分别与水和乙醇反应 |
| B |
欲证明CH2=CHCHO中含有碳碳双键 |
滴加酸性KMnO4溶液,看紫红色是否褪去 |
| C |
欲确定磷、砷两元素非金属性的强弱 |
测定同温同浓度的Na3PO4和Na3AsO4水溶液的pH |
| D |
欲除去苯中混有的苯酚 |
向混合液中加入NaOH溶液,充分反应后,分液 |