(1)为了达到下表中的实验要求,请从“供选择的化学试剂及方法”栏中,选择正确选项的字母代号填入对应的空格中。
| 序号 |
实验要求 |
答案 |
供选择的化学试剂及方法 |
| a |
检验乙酸是否具有酸性 |
|
A.新制的氢氧化铜悬浊液 |
| b |
检验植物油中是否含有碳碳双键 |
|
B.紫色石蕊试液 |
| c |
检验尿液中是否含有葡萄糖 |
|
C.加入饱和Na2CO3溶液,分液 |
| d |
除去乙酸乙酯中的少量乙酸 |
|
D.溴水 |
(2)A的结构简式如下:A分子中两种含氧官能团的名称是 、 。

请写出该物质与足量的金属钠发生反应的化学方程式 。
用软锰矿(主要成分为MnO2)生产高锰酸钾产生的锰泥中,还含有18%的MnO2、3%的KOH(均为质量分数),及少量Cu、Pb的化合物等,用锰泥可回收制取MnCO3,过程如下图: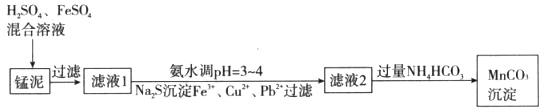
(1)锰泥中加入H2SO4、FeSO4混合溶液,反应的离子方程式是__________。
(2)经实验证明:MnO2稍过量时,起始H2SO4、FeSO4混合溶液中c(H+)/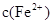 <0.7时,滤液1中能够检验出有Fe
<0.7时,滤液1中能够检验出有Fe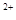 ;
;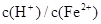 ≥0.7时,滤液1中不能检验出有Fe2+。
≥0.7时,滤液1中不能检验出有Fe2+。
①检验Fe2+是否氧化完全的实验操作是__________。
②生产时H2SO4、FeSO4混合溶液中c(H+)/c(Fe2+)控制在0.7~1之间,不宜过大,请从节约药品的角度分析,原因是__________。
若c(H+)/c(Fe2+)>1,调节c(H+)/c(Fe2+)到0.7~1的方法是__________。
(3)写出滤液2中加入过量NH4HCO3反应的离子方程式__________。
(4)上述过程锰回收率可达95%,若处理1740 kg的锰泥,可生产MnCO3__________kg(已知相对分子质量:MnO2 87;MnCO3 115)。
减少二氧化碳的排放是一项重要课题。
(1)CO2经催化加氢可合成低碳烯烃: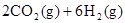

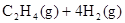
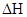
在0.1 MPa时,按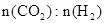 =1:3投料,如图所示不同温度(T)下,平衡时的四种气态物质的物质的量(n)的关系。
=1:3投料,如图所示不同温度(T)下,平衡时的四种气态物质的物质的量(n)的关系。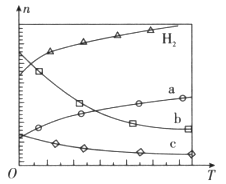
①该反应的△H__________0(填“>”、“=”或“<”)。
②曲线b表示的物质为__________。
③为提高CO2的平衡转化率,除改变温度外,还可采取的措施是__________。
(2)在强酸性的电解质水溶液中,惰性材料做电极,电解CO2可得到多种燃料,其原理如下图所示。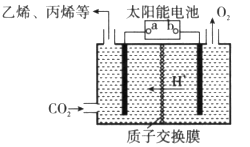
①该工艺中能量转化方式主要有__________。
②b为电源的__________(填“正”或“负”)极,电解时,生成乙烯的电极反应式是__________。
(3)以CO2为原料制取碳(C)的太阳能工艺如图所示。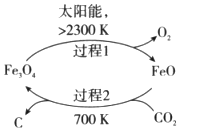
①过程1每反应1mol Fe3O4转移电子的物质的量为__________。
②过程2发生反应的化学方程式是__________。
(4分)某化合物2.3g在足量的氧气中充分燃烧,只生成了4.4g CO2和2.7gH2O。该化合物的相对分子质量是氢气相对分子质量的23倍。该化合物的分子式为________________;若该化合物的1H核磁共振谱只有一个信号峰,则其结构简式为________________。
(6分)某有机物A结构如下: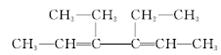
(1)用系统命名法对其命名:_____________________________________________
若该烃完全氢化后再与氯气光照下进行反应,其一氯代物有______种。
(2)烃B与烃A是同分异构体,能使酸性高锰酸钾溶液和溴水褪色,其一氯取代物只有一种结构,烃B的结构简式可以为_______________________________
(8分)已知某有机物的相对分子质量为58,请回答:
(1)若该有机物为烃,且含有支链,则其结构简式为____________________________
(2)若为结构中只含1个-CH3和一个官能团的含氧衍生物,则官能团的名称为_______
(3)若为结构中有2个 — CH3含氧衍生物,则可能的结构简式为_________________
(4)若分子中有 — OH,无C=O键,则结构简式为_____________________________