下列条件下,可以大量共存的离子组是
| A.某无色溶液中:Na+、Cu2+、Cl-、MnO4- |
| B.含有大量Fe3+的溶液中:Na+、SO42-、K+、SCN-- |
| C.含有大量NH4+的溶液中:Ba2+、K+、Cl-、OH- |
| D.在pH=1的溶液中:K+、Fe3+、Cl-、NO3- |
下列反应中,属于加成反应的是
A.CH4+C12 CH3C1+HC1 CH3C1+HC1 |
B.CH2=CH2+Br2 →CH2BrCH2Br |
| C.2C2H5OH+2Na→2C2H5ONa+H2↑ | D.C2H5OH+3O2 2CO2+3H2O 2CO2+3H2O |
某化学反应中,反应物B的物质的量浓度在20s内,从2.0mol/L变成了1.0mol/L,则这20s内B的反应速率为
A.0.05mol/(L s) s) |
B.0.05 | C.0.5mol/(L s) s) |
D.0.05mol/L |
下列各组物质中,可以用分液漏斗分离的一组是
| A.酒精和碘 | B.苯和水 | C.乙酸和水 | D.溴和四氯化碳 |
下列对应符号表述正确的是
| A.一氯甲烷的结构式CH3C1 | B.苯的分子式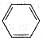 |
| C.葡萄糖的结构简式C6H12O6 | D.丙烷分子的球棍模型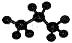 |
下列物质中,在一定条件下既能发生加成反应,也能发生取代反应,但不能使KMnO4酸性溶液褪色的是
| A.乙烷 | B.苯 | C.乙烯 | D.乙醇 |