一定温度下,在容积固定的V L密闭容器中加入n mol A、2n mol B,发生反应:A(g)+2B(g) 2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x。
2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x。
(1)一段时间后上述反应达到平衡。则下列说法中正确的是________(填字母)。
A.物质A、B的转化率之比为1∶2
B.起始时刻和达到平衡后容器中的压强之比为3n∶(3n-nx)
C.充入惰性气体(如Ar),平衡向正反应方向移动
D.当2v正(A)=v逆(B)时,反应一定达到平衡状态
(2)K和x的关系满足K=____________。
(3)该反应的逆反应速率与时间的关系如图所示。
①由图可知,反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的条件:
t2时_________________________;
t8时_________________________。
②t2时平衡向__________(填“正反应”或“逆反应”)方向移动。
③若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线。
(每空2分,共12分)(1)用NA代表阿伏加德罗常数,在C2H2(g)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650 kJ的热量。其热化学方程式为___________________________。
(2)已知拆开1 mol H-H键、1mol N-H键、1mol N≡N键分别需要的能量是436 kJ,391kJ,946 kJ,则N2和H2反应生成NH3的热化学方程式为______________________。
(3)实验室有PH=4的盐酸、硫酸、醋酸三瓶溶液:(以下用“>、=、<”表示)
① 若取相同体积的上述三种酸分别加入蒸馏水稀释至PH=6,需要水的体积依次为V1、 V2、V3则其关系为。
② 若完全中和体积和物质的量浓度均相同的Ba(OH)2,需上述三种酸的体积依次为V1、V2、V3,则其关系是。
③ 若取同体积的上述三种酸溶液分别加入足量的锌粉,反应开始放出H2的速率依次为v1,v2,v3,则其关系是;相同状况下产生气体体关系是__________ (用V1、V2、V3表示)。
(9分)实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理4NH4++6HCHO=3H++6H2O+(CH2)6N4H+(滴定时,1 mol(CH2)6N4H+与 l mol H+相当),然后用NaOH标准溶液滴定反应生成的酸,某兴趣小组用甲醛法进行了如下实验:
步骤I:称取样品1.500g。
步骤II:将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ:移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴 酚 酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数__________(填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积_________(填“偏大”、“偏小”或“无影响”)。
③滴定时边滴边摇动锥形瓶,眼睛应观察。
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚 酞指示剂由色变成色。
(2)滴定结果如下表所示: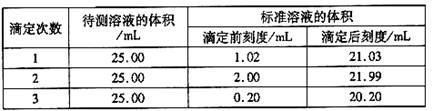
若NaOH标准溶液的浓度为0.1010mol·L-1则该样品中氮的质量分数为 。
(8分)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。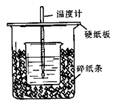
通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是。
(2)烧杯间填满碎纸条的作用是。
(3)大烧杯上如不盖硬纸板,求得的中和热数值(填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热(填“相等、不相等”),简述理由
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会;(填“偏大”、“偏小”、“无影响”)。
(共6分)海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验: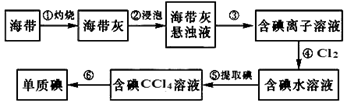
请填写下列空白:
(1)步骤⑤的操作名称是,除烧杯外,还必须用到的仪器是:从碘水溶液中提取碘,还可以选用下列(填字母)物质作为萃取剂。
A.酒精B.苯(密度比水小) C.KI溶液
(2)步骤③的实验操作名称是
(3)步骤④中反应的化学方程式是
(4)步骤⑥的目的是从含碘的四氯化碳溶液中分离出单质碘和回收四氯化碳,该步骤的实验操作名称是。
化合物G是中药黄芩中的主要活性成分之一,具有氧化和抗肿瘤作用。G的合成路线如下图所示:
已知D的结构简式为: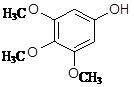
回答下列问题:
(1)写出G中含氧官能团的名称;G的分子式为。
(2)反应③的反应类型是反应(填“取代”、“加成”或“消去”);
(3)同时符合下列条件的D的同分异构体有多种,请写出其中一种的结构简式。
a.属于苯的衍生物,苯环上共有4个取代基;
b.核磁共振氢谱中有5种等效氢;
c.与FeCl3溶液发生显色反应
(4)在反应①中,反应物的物质的量之比为l:1,反应的化学方程式为
若M呈酸性,则M的结构简式为。
(5)请运用所学,任选无机试剂,由 为原料合成苯甲醛
为原料合成苯甲醛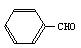 。
。
(合成路线流程图示例如下: