A、B、C、D、E是同周期元素,A、B的最高价氧化物的水化物呈碱性,且B比A的碱性强,C、D最高价氧化物水化物是酸,且C比D的酸性强,E是这五种元素中原子半径最大的,则它们的原子序数由小到大的顺序是
A.E、C、D、B、A B.D、B、C、A、E
C.E、B、A、D、C D.A、B、C、D、E
2005年,全球发生了禽流感。我国科学家发现金丝桃素对高致病性禽流感病毒杀灭效果良好,某种金丝桃素的结构式为:

下列有关金丝桃素说法错误的是
| A.分子式为C17H23NO3 |
B.可以发生加成、酯化等反应 |
| C.苯环上的一氯取代物有3种 |
| D.金丝桃素常温常压下为气态 |
2002年诺贝尔化学奖获得者的贡献之一是发明了对有机物分子进行结构分析的质谱法。其方法是让极少量的(10-9g)化合物通过质谱仪的离子化室使样品分子大量离子化,少量分子碎裂成更小的离子。如C2H6离子化后可得到C2H6+、C2H5+、C2H4+,然后测定其质荷比。某有机物样品的质荷比如图所示。该有机物可能是
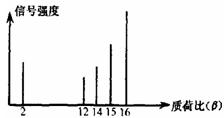
| A.甲醇 | B.甲烷 | C.丙烷 | D.乙烯 |
下列分子式表示的物质一定是纯净物的是
| A.C5H10 | B.C7H8 | C.CH4O | D.C2H4Cl2 |
下列有机物命名正确的是
1,3,4-三甲苯 2-甲基-2-氯丙烷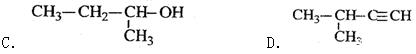
2-甲基-1-丙醇 2-甲基-3-丁炔
下列物质属于天然高分子化合物的是
| A.聚乙烯 | B.合成橡胶 | C.油脂 | D.纤维素 |