化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:

已知:RCHO+CH3COOR’ RCH=CHCOOR’ 请回答:
RCH=CHCOOR’ 请回答:
(1)A中官能团的名称是 ;C→D的反应类型为 。
(2)B+D→F的化学方程式 。
(3)E的结构简式 。
(4)对于化合物X,下列说法正确的是 。
| A.能发生水解反应 | B.能发生银镜反应 |
| C.不与浓硝酸发生取代反应 | D.能使Br2的CCl4溶液褪色 |
(5)F有多种同分异构体,含有酯基和一取代苯结构的同分异构体有五个,其中四个的结构简式是

请写出另外一个同分异构体的结构简式 。
苹果酸是一种常见的有机酸,其结构简式如右图所示: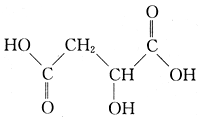
(1)苹果酸的分子式为_____________。
(2)苹果酸分子中所含的官能团名称是____________。
(3)苹果酸可以发生的化学反应有_______(填序号)。
①水解反应 ②取代反应 ③氧化反应 ④加聚反应
(4)1 mol苹果酸与足量的钠反应最多产生________mol氢气。
(5)假定苹果酸与乙酸按照物质的量1:1发生酯化反应,写出对应的化学方程式:______。
短周期元素X、Y、Z、M、N原子序数依次增大,有关信息如下:
请回答:
(1)X2Z的电子式是________;M2Z中所含化学键类型是________。
(2)Y的非金属性比N__________(填“强”或“弱”),能证明此结论的事实是_________(用离子方程式表示)。
(3)YX4的结构简式为________;分子里各原子的空间分布具有________结构;在光照的条件下,将1 mol YX4与1 mol Cl2混合充分反应后,得到的产物最多有______种。
现代生活离不开铝,铝有许多优良的性能,因此在各方面有极其广泛的用途。
(1)在高温下,氧化铁粉末发生铝热反应的化学方程式为____________。
(2)某学生拟用铝粉制备少量Al(OH)3,制备过程如下图所示:
请回答:
①通过操作a分离出Al(OH)3,操作a的名称是________。
②从Al(OH)3的性质考虑,用Al2(SO4)3溶液制备Al(OH)3时,常用氨水而不用NaOH溶液,请用
一个化学方程式表明其理由:______________。
(3)铝可以和烧碱溶液反应,该反应的离子方程式为______________。
(4)工业上冶炼的化学方程式为________;若生产2.7t铝,则转移电子的物质的量为_______。
化学反应与能量密不可分,回答下列问题。
(1)已知31g白磷变为31g红磷时释放能量。试回答:
①上述变化属于____化学(填“物理”或“化学”)变化。
②31g白磷的能量_____(“>”或“<”)31g红磷的能量。
(2)A、B、C三个烧杯中分别盛有200mL相同物质的量浓度的稀硫酸:
①分别写出B、C装置中铁片表面发生反应的电极反应式:
B______________________,C____________________。
②一段时间后,C中产生3.36L(标准状况下)气体时,硫酸恰好消耗完。此时,三个烧杯中液体质量由大到小的顺序为________(填字母),稀硫酸的物质的量浓度为________mol/L。
X、Y、Z、M、R、Q是短周期主族元素,部分信息如下表所示: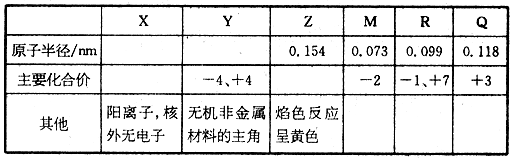
(1)R在自然界中有质量数为35和37两种核素,它们之间的关系互为__________,R在元素周期表中的位置是________。
(2)Z的单质与水反应的离子方程式是______________。
(3)Y与R相比,非金属性较强的是_______(用元素符号表示),下列事实能证明这一结论的是______(选填字母序号)。
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性XR>YX4
c.Y与R形成的化合物中Y呈正价
(4)根据表中数据推测,Y的原子半径的最小范围是________。