下列有关化学用语表示正确的是
A.水分子的球棍模型: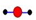 |
B.S2-的结构示意图: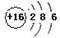 |
C.质子数为53,中子数为78的碘原子: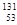 I I |
D.N2的电子式: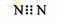 |
下列反应:①金属钠在纯氧中燃烧②FeSO4溶液中滴入NaOH溶液并在空气中放置一段时间 ③FeCl3溶液中滴入KSCN溶液,其产物颜色按红、红褐、淡黄的顺序排列的是
| A.②③① | B.③②① | C.③①② | D.①②③ |
下列实验可行的是
| A.用酒精萃取碘水中的碘 |
| B.加入盐酸以除去硫酸钠溶液中的少量碳酸钠杂质 |
| C.加热氯化铵与氢氧化钙的固体混合物制取氨 |
| D.在容量瓶中加入少量的水,再加入浓硫酸配制一定物质的量浓度的稀硫酸 |
下列物质中,不能使有色布条褪色的是
| A.氯水 | B.次氯酸钠溶液 | C.漂白粉溶液 | D.氯化钙溶液 |
下列情况会对人体健康造成较大危害的是
| A.自来水中通入少量Cl2进行杀菌、消毒 |
| B.用SO2漂白食品 |
| C.用食醋清洗热水瓶胆内壁附着的水垢(CaCO3) |
| D.用小苏打(NaHCO3)发酵面团制作馒头 |
下列单质中,遇到盐酸或强碱溶液都能放出氢气的是
| A.Cu | B.Fe | C.Al | D.Si |