下列反应的离子方程式书写正确的是
| A.将Al条投入NaOH溶液中:Al+OH-+H2O === AlO2-+H2↑ |
| B.铜溶于稀硝酸中:Cu+4H++2NO3-=== Cu2++2NO2↑+2H2O |
| C.碳酸氢钙溶液中加入过量的氢氧化钠溶液:HCO3-+OH- === CO32-+H2O |
| D.向碳酸钠溶液中逐滴加入与之等体积等物质的量浓度的稀醋酸:CO32-+CH3COOH === CH3COO-+HCO3- |
下列叙述中,正确的是( )
| A.水泥、玻璃、水晶饰物都是硅酸盐制品 |
| B.用澄清石灰水鉴别SO2和CO2 |
| C.将Fe(NO3)2溶于稀盐酸,滴加KSCN 溶液没有颜色变化 |
| D.透闪石的化学成分为Ca2Mg5Si8O22(OH)2写成氧化物的形式为:2CaO·5MgO·8SiO2·H2O |
能用H+ + OH- =H2O 来表示的化学反应是( )
| A.固体C u ( O H ) 2和H2SO4溶液反应 |
| B.澄清石灰水和HNO3溶液反应 |
| C.KOH 溶液和醋酸溶液反应 |
| D.Ba(OH)2溶液和H2SO4溶液反应 |
以下实验装置一般不用于分离物质的是( )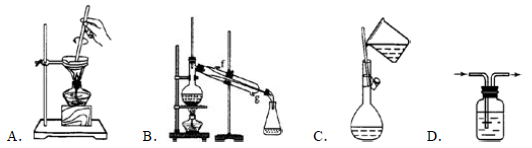
为了检验某氯化亚铁溶液是否变质,最好向溶液中加入
| A.NaOH 溶液 | B.铁片 | C.KSCN 溶液 | D.石蕊试液 |
下列各种冶炼方法中,可制得相应金属的为( )
| A.加热氧化钠 | B.电解熔融氯化镁 |
| C.氧化铝与一氧化碳高温反应 | D.氯化钠与铝粉高温共热 |