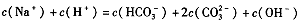某反应体系中存在下列六种物质:As2S3、HNO3、H2SO4、NO、H3AsO4和H2O,已知其中As2S3是反应物之一。下列说法不正确的是
| A.该反应属于氧化还原反应 |
| B.此反应中只有砷元素被氧化,只有氮元素被还原 |
| C.HNO3、H2O是反应物,H2SO4、NO、H3AsO4是生成物 |
| D.HNO3、H2SO4、H3AsO4都是最高价氧化物对应的水化物 |
把a L硫酸铵和硝酸铵混合液分成两等份,一份需用b mol烧碱刚好把氨全部赶出,另一份与BaCl2溶液反应恰好消耗c mol BaCl2。原溶液中NO3-的物质的量浓度是()
A.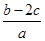 mol·L-1 mol·L-1 |
B.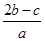 mol·L-1 mol·L-1 |
C.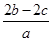 mol·L-1 mol·L-1 |
D.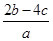 mol·L-1 mol·L-1 |
下列操作中,完全正确的一组是( )
①用试管夹夹持试管时,试管夹从试管底部往上套,夹在试管的中上部
②给盛有液体的体积超过1/3容积的试管加热
③把鼻孔靠近容器口去闻气体的气味
④将试管平放,用纸槽往试管里送入固体粉末后,然后竖立试管
⑤取用放在细口瓶中的液体时,取下瓶塞倒放在桌面上,倾倒液体时,瓶上的标签对着地面
⑥将烧瓶放在桌上,用力塞紧塞子
⑦用坩埚钳夹取加热后的蒸发皿
⑧将滴管垂直伸进试管内滴加液体
⑨稀释浓硫酸时,把水迅速倒入盛有浓硫酸的量筒中
⑩检验装置的气密性时,把导管的一端浸入水中,用手捂住容器的外壁或用酒精灯微热
| A.①④⑦⑩ | B.①④⑤⑦⑩ | C.①④⑤⑦⑧⑩ | D.④⑤⑦⑩ |
下列实验操作使测定(或配制)结果偏高的是( )
| A.配制一定物质的量浓度的溶液,定容时俯视刻度线 |
| B.测量一包固体的质量,将药品放在右盘,砝码放在左盘,并需移动游码使之平衡 |
| C.中和滴定用的锥形瓶加入待测液后,再加少量蒸馏水稀释 |
| D.在敞口容器中测量氢氧化钠和稀盐酸反应的中和热 |
用石墨电极电解CuCl2溶液(见图)。下列分析正确的是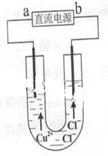
| A.a端是直流电源的负极 |
| B.通电使CuCl2发生电离 |
| C.阳极上发生的反应:Cu2++2e-=Cu |
| D.通电一段时间后,在阴极附近观察到黄绿色气体 |
足量的二氧化碳通入到1mol/L NaOH溶液中,下列说法错误的是
| A.溶液中Na+离子个数为NA(NA表示阿伏加德罗常数) |
| B.溶液中的CO32—离子浓度先增大后减小 |
| C.微热反应后的溶液,溶液的pH会升高 |
| D.当恰好生成Na2CO3时,溶液中离子浓度大小存在以下关系: |