(10分)分子式为C2H6O的化合物A具有如下性质:
A+Na―→慢慢产生气泡
A+CH3COOH 有香味的产物
有香味的产物
(1)根据上述信息,对该化合物可作出的判断是( )。
| A.一定含有—OH | B.一定含有—COOH |
| C.A为乙醇 | D.A为乙酸 |
(2)含A的体积分数为75%的水溶液可以用作___________________
(3)A与钠反应的化学方程式:__________________
(4)化合物A和CH3COOH反应生成的有香味的产物的结构简式为________。
(5)A可由含淀粉[(C6H10O5)n]的农产品如玉米、小麦、薯类等经发酵、蒸馏而得。请写出淀粉水解的化学方程式:__________________
下列各组物质中
1.丁烷和2—甲基丙烷 2.甲烷和丁烷 3.35Cl和37Cl 4.金刚石和石墨
(用序号填空)是同分异构体;是同素异形体;是同位素;是同系物。
请根据官能团的不同对下列有机物进行分类。

(1)芳香烃:;(2)卤代烃:;
(3)醇:;(4)酚:;
(5)醛:;(6)酮:;
(7)羧酸:;(8)酯:。
医院抢救重金属中毒的病人时会采取哪些措施?常用的消毒方法有哪些?
(1),。
(2)有关葡萄糖反应的特征现象表现为:
与新制Cu(OH)2反应:。
与银氨溶液反应:。
(3)含碳原子数少于或等于10的烷烃中,其一氯代物只有一种的烷烃共有____种。
X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y、E的元素符号依次为、_______、 ____ ;
(2)XZ2与YZ2分子的立体结构分别是和,
相同条件下两者在水中的溶解度较大的是
(写分子式),理由是;
(3)Q的元素符号是,它属于第周期,
它的核外电子排布式为,在形成化合物时,它的最高化合价为.
某离子晶体晶胞如图所示,阳离子 X(●)位于立方体的顶点,阴离子Y(○)位于立方体的中心,试分析: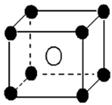
(1)晶体中Y的配位数是; X的配位数是;该晶体的化学式为 。
(2)晶体中在每个X周围与它最接近且距离相等的X共有个。
(3)该晶体的摩尔质量为M g/mol,晶体密度为ρ g/cm3,阿伏加德罗常数为NA,则晶体中两个距离最近的X中心间的距离为 cm。