反应(1)、(2)分别是从海藻灰和智利硝石中提取碘的主要反应:
(1)2NaI+MnO2+3H2SO4====2NaHSO4+MnSO4+2H2O+I2
(2)2NaIO3+5NaHSO3====2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是
| A.两个反应中NaHSO4均为氧化产物 |
| B.I2在反应(1)中是还原产物,在反应(2)中是氧化产物 |
| C.氧化性:MnO2>SO42->IO3- >I2 |
| D.反应(1)、(2)中生成等量的I2时转移电子数之比为1∶5 |
实验宣制取少量干燥的氨气涉及下列装置,其中正确的是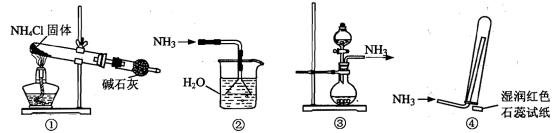
| A.①是氨气发生装置 | B.③是氮气发生装置 |
| C.②是氨气吸收装置 | D.④是氨气收集、检验装置 |
下图所示最验证氯气性质的徼型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O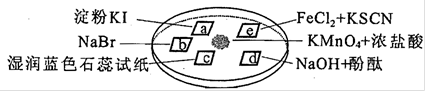
对实验现象的“解释或结论”正确的是
| 选项 |
实验现象 |
解释或结论 |
| A |
a处变蓝,b处变红棕色 |
氧化性:Cl2>Br2>I2 |
| B |
c处先变红,后褪色 |
氯气与水生成了酸性物质 |
| C |
d处立即褪色 |
氯气与水生成了漂白性物质 |
| D |
e处变红色 |
还原性:Fe2+>Cl- |
下列关于硫酸工业生产过程的叙述错误的是
| A.在接触室中使用铁粉作催化剂 |
| B.在接触室中运用热交换技术可充分利用能源 |
| C.把硫铁磨成细粉末,可以提高原料的利用率 |
| D.该反应采用450~500℃主要是因为该温度下催化剂活性好 |
下列陈述正确并且有因果关系的是
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
SO2有漂白性 |
SO2可使溴水褪色 |
| B |
SiO2有导电性 |
SiO2可用于制备光导纤维 |
| C |
浓硫酸有强氧化性 |
浓硫酸可用于干燥H2和CO |
| D |
Fe3+有强氧化性 |
FeCl3溶液可用于回收废旧电路板中的铜 |
将足量X气体通入Y溶液中,实验结果与预测的现象一致的组合是
| A.只有①②③ | B.只有①②④ |
| C.只有①③④ | D.①②③④ |