下图是由常见元素组成的一些单质及其化合物之间的转化关系图。常温常压下,B、E、F、H、I均为气体,F为无色无味,且能使澄清石灰水变浑浊;B、E、I均有刺激性气味,E能使湿润的红色石蕊试纸变蓝,B、E在空气中相遇会产生白烟,I为红棕色。A是一种常见的肥料。C、G、K的焰色反应呈黄色。(反应中生成的部分物质已略去)
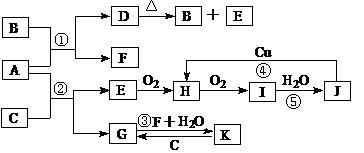
请回答下列问题:
(1)物质D的化学式为 ;
(2)写出反应③的化学方程式 ;
(3)写出反应④的离子方程式 ;
(4)写出反应⑤的化学方程式,并在方程式上标出电子转移的方向和数目 。
A、B、C、D、E、F为常见的原子序数依次增大的短周期元素,B、C、D、E、F的简单离子的电子层结构相同,A和E同主族,且原子的最外层电子数的关系为A+D=B+F=8。请回答:
(1)试写出B2单质的电子式为           。试写出由上述元素组成的分子中含有4个原子核且为18电子结构的物质的化学式               。
(2)含F元素对应的金属阳离子的溶液中滴加过量E的最高价氧化物对应水化物的溶液,其离子方程式是                           。
(3)已知B2A4与BA3具有相似的性质,B2A4通过炽热的氧化铜粉末,粉末由黑色变为红色单质,且产物对大气无污染,其化学反应方程式是                             。
(4)在2 L的密闭容器中,通入2 mol B2气体和3 mol A2气体,一定温度下反应生成BA3气体,当反应达到平衡时,A2的浓度为0.15 mol·L-1,同时放出约83.2 kJ的热量,该反应的热化学方程式为                                                       。
(5)已知某化合物EB3与水可以反应生成两种气体单质和一种碱,试写出其化学方程式              ;若0.1 mol该化合物完全反应,转移电子的物质的量为             。
如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物,已知:
①反应C+G  B+H能放出大量的热,G是红综色固体粉末;
B+H能放出大量的热,G是红综色固体粉末;
②I是一种常见的温室气体,它和E可以发生反应:2E+I  2F+D,F中的E元素的质量分数为60%.
2F+D,F中的E元素的质量分数为60%.
回答问题:
(1)①中反应的化学方程式为______________________________;
(2)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,至少需要铜粉__________克;
(3)C与过量NaOH溶液反应的离子方程式为________________________________,
反应后的溶液与过量的化合物I反应的离子方程式为_______________________;
(4)E与I反应的化学方程式为______________________________;
(5)写出H物质在工业上的一种用途___________________;
(6)将一定量的B完全溶于过量盐酸中,然后通入0.005mol Cl2,再加入0.01mol重铬酸钾晶体(K2Cr2O7),恰好使溶液中B2+全部转化为B3+,铬元素本身被还原为+3价铬离子。通过计算确定原B的物质的量为______。
A.0.01mol B.0.03mol C.0.04mol D.0.07mol
[化学—选修5:有机化学基础]化合物H的分子中含有醛基和酯基。H可以用C和F在一定条件下合成(如图):
已知以下信息:
①A的核磁共振氢谱中有三组峰;且能与饱和碳酸氢钠溶液反应放出CO2。
② 。
。
③化合物D苯环上的一氯代物只有两种。
④通常同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
(1)A的化学名称_____________________;
(2)B的结构简式为_____________________;
(3)D生成E的化学方程式为_____________________,该反应类型为______________;
(4)F的结构简式为______________;
(5)H在一定条件下反应生成高聚物的化学方程式为______________;
(6)F的同系物G比F相对分子质量大14,G的同分异构体中能同时满足如下条件:①苯环上只有两个取代基;②不能使FeCl3溶液显色,共有_______种(不考虑立体异构)。G的一个同分异构体被酸性高锰酸钾溶液氧化后核磁共振氢谱为两组峰,且峰面积比为2:1,写出G的这种同分异构体的结构简式为________。
A、B、C、D、E、F、G是原子序数依次增大的短周期主族元素,A的原子核内无中子,B、F在元素周期表中的相对位置如图,B与氧元素能形成两种无色气体,D是地壳中含量最多的元素,E是地壳中含量最多的金属元素。
| B |
||
| F |
(1)BF2的结构式为____________。
(2)D和F的氢化物中沸点较高的是_________(填化学式)。
(3)实验室制取G2气体的离子方程式为______________。
(4)在微电子工业中,C的最简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为____________________。
(5)FD2气体通入BaCl2和C的最高价氧化物对应的水化物的混合溶液中,生成白色沉淀和无色气体,有关反应的离子方程式为___________________________________________________。
(6)火箭使用B2A8C2作燃料,N2O4为氧化剂,燃烧放出的巨大能量能把火箭送入太空,并且产生三种无污染的气体,其化学方程式为_______________________.
(7)上述元素可组成盐Q:CA4E(FD4)2。向盛有20mL0.5mol/LQ溶液的烧杯中加入12mL2.0mol/LBa(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为_________。
【化学—选修5:有机化学基础】
对乙酰氨基苯酚M( )是最常见的消炎解热镇痛药,用于治疗感冒发烧和关节痛等。M的一种合成路线如下:
)是最常见的消炎解热镇痛药,用于治疗感冒发烧和关节痛等。M的一种合成路线如下: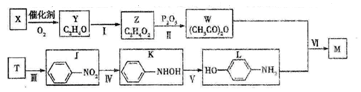
已知:①X、Y、T分子的核碰共振氢谱只显示1组峰,且X能使溴水褪色;
②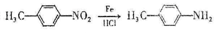 。
。
(1)X、Y的结构简式为______________、_____________________;
(2)Ⅲ的反应类型为_______________,Ⅵ的反应方程式为________________;
(3)M与足量氢氧化钠溶液反应的化学方程式为______________________________;
(4)M有多种同分异构体,其中一类与J互为同系物且氮原子与苯环直接相连,此类同分异构体共有_____种;另一类同分异构体同时满足下列条件①属于对位二取代苯且苯环上连有—NH2;②能发生水解反应;③核碰共振氢谱有4组峰。写出其中一种同分异构体的结构简式_________________。